本研究通过在体电生理记录、钙成像、光遗传学操控和行为学分析等技术,揭示了小鼠嗅球中 僧帽/簇状细胞(M/T)细胞编码先天恐惧的神经机制。研究发现,捕食者气味(nTMT)可引发 M/T 细胞产生增强、抑制和无反应三种活动模式。其中,抑制性反应神经元编码主动逃避行为,而增强和抑制性反应神经元共同编码被动僵硬行为。其中逃避和僵硬行为的识别与衡量由一湾生命科技核心的 BehaviorAtlas 3D-AI 动物行为分析系统助力!
先天恐惧是动物赖以生存的基础本能,而嗅觉是啮齿类动物感知捕食者威胁的主要途径。面对威胁气味时,啮齿动物表现出主动逃避和被动僵硬 等恐惧行为。嗅球作为处理嗅觉信息的第一站,其输出神经元( M/T 细胞)如何将特定的气味信息转化为不同的恐惧行为,其具体的神经编码机制尚不清楚。此前的研究虽然知道嗅球参与恐惧反应,但在可以自由活动的动物中,很难将复杂的行为精确地与特定神经元的活动模式对应起来 ,也缺乏对背后分子机制的了解。
2025 年 9 月 23 日,南京医科大学卢应梅 / 韩峰 / 毛兴峰团队在《 Cell Reports 》发表了题为 “ Multimode neural population coding of diverse innate fear response by mitral and tufted cells ” 的研究论文。该研究通过结合在体电生理记录、钙成像、光遗传学操控和高精度 3D-AI 行为学分析 等多种技术,系统地研究了小鼠大脑处理先天恐惧气味信息的嗅球神经编码机制,将 M/T 细胞的活动模式与特定的恐惧行为对应起来。研究表明,编码先天恐惧的过程与 Cdk5 的表达直接相关,Cdk5 的缺失会损害 M/T 细胞的正常放电活动,导致恐惧反应减弱。总而言之,这项工作解决了嗅觉系统如何编码不同强度的先天恐惧行为这一关键科学问题,从神经环路活动模式到关键分子的层面,为理解先天恐惧的神经基础提供了全新的、更为精细的认知框架。
01 识别多元编码模式:增强、抑制和无反应三种模式
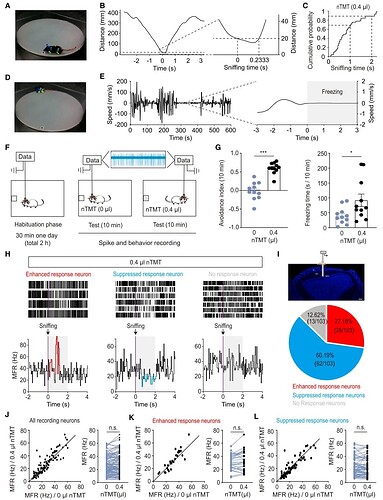
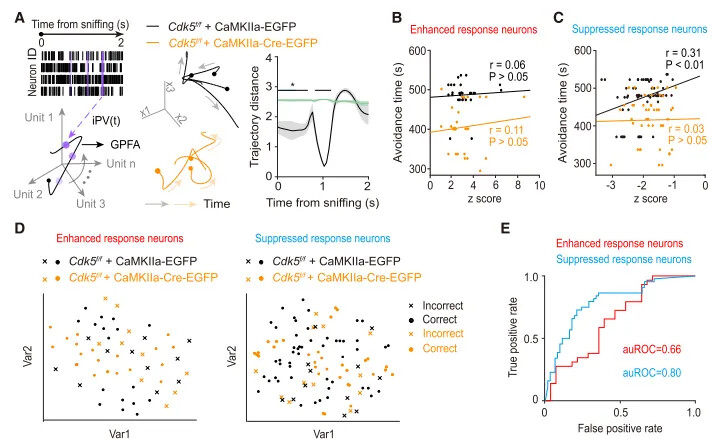
在理解 M/T 细胞如何处理先天恐惧信息方面,一个主要障碍是无法在自由活动的动物中精确区分各种感觉线索(sensory cues)的贡献。为此,研究者采用 BehaviorAtlas 3D-AI 动物行为分析系统 ,结合在体电生理记录,来解码特定恐惧行为中的 M/T 细胞活动。在旷场中放置 nTMT(捕食者的气味后),会引起老鼠的先天恐惧反应。 3D-AI 行为系统精准识别并量化出小鼠的主动逃避和被动僵硬行为显著增加(图1G)。与此同时,M/T 细胞呈现出三种截然不同的反应模式:增强反应型、抑制反应型和无反应型 (图1H)。其中,在小鼠表现出回避行为时,抑制反应模式占比最大(图1I)。
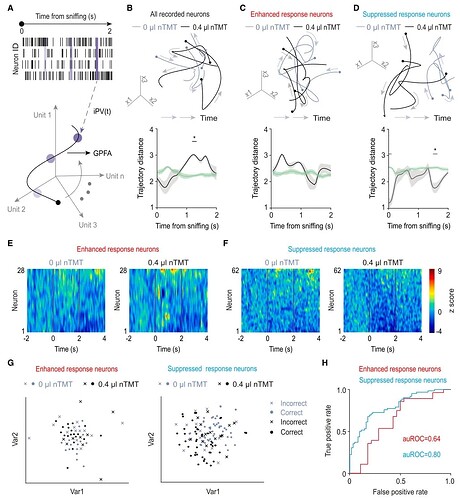
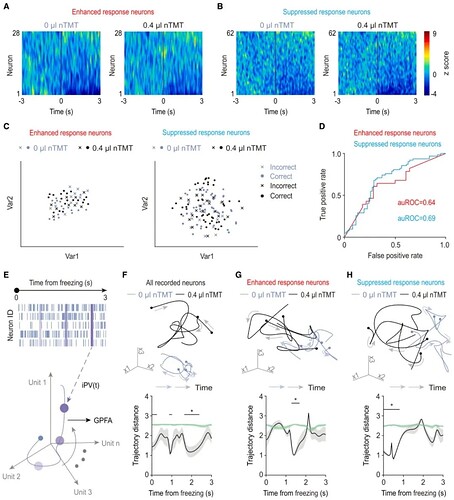
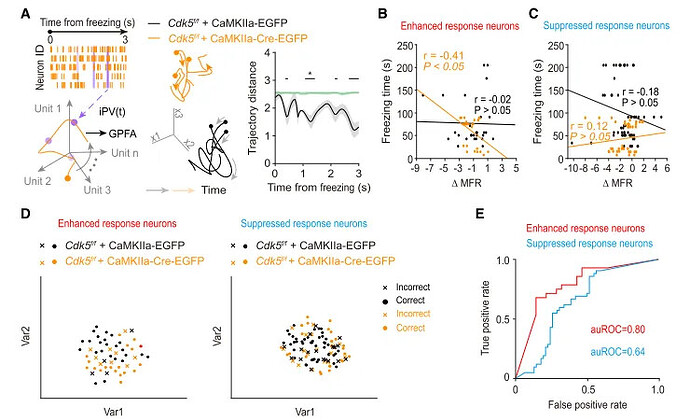
进一步地,研究者运用高斯过程因子分析(GPFA)可视化 M/T 细胞群体的活动“轨迹”,发现不同的恐惧行为表现出不同的 M/T 细胞活动模式,在主动逃避期间,仅“抑制”神经元的轨迹显著变化,而在被动僵硬期间,“增强”和“抑制“神经元的轨迹均显著变化(图2A-D,图3E-H)。同时,结合 K- 最邻近(KNN)分类器发现,神经元活动的“抑制”是编码主动回避的关键信号,而“抑制”和“增强”两种活动的组合则共同编码了被动僵硬行为 (图2E-H,图3A-D)。这揭示了一种精细的、多模式的神经群体编码策略。
02 揭示关键机制:Cdk5 分子的缺失损害了 M/T 细胞活性
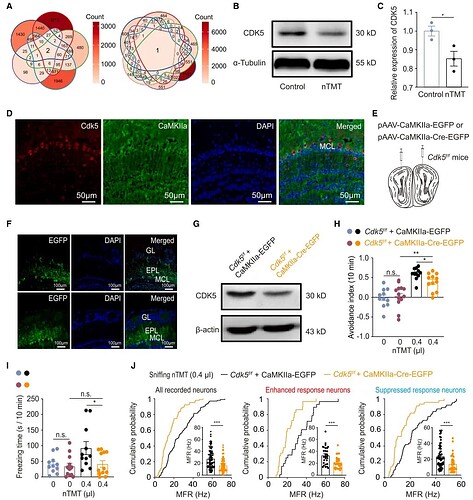
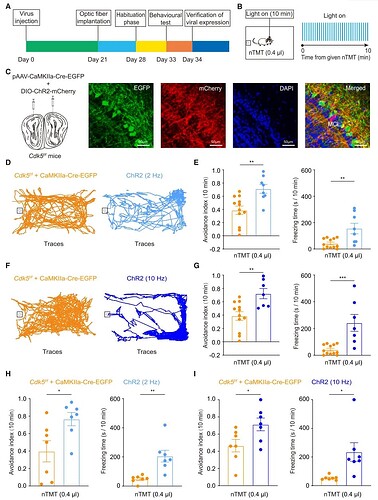
为了进一步探索调控 M/T 细胞编码先天恐惧的关键机制,研究者通过生物信息学分析锁定了 Cdk5 是与嗅觉和先天恐惧高度相关的分子,并发现 nTMT 诱导的先天恐惧会下调 Cdk5 的蛋白水平(图4A-C)。在 M/T 细胞中特异性敲除 Cdk5 后,小鼠对 nTMT 的逃避行为和僵硬行为均显著减少(图4G-I),并且其 M/T 细胞的平均放电频率也显著降低(图4J),表明 Cdk5 分子的缺失损害了 M/T 细胞活性,进而削弱了先天恐惧反应。
随后,为深入探究 Cdk5 缺失如何影响不同恐惧行为的细胞编码,发现 Cdk5 在编码不同恐惧行为时具有特异性:它主要通过影响“抑制”反应 M/T 细胞的活动来调节回避行为;同时通过影响“增强”反应 M/T 细胞的活动来调节僵硬行为 (图5、6)。这些结果说明,Cdk5 调控着两种不同的恐惧行为输出,是维持 M/T 细胞正常功能和执行恐惧编码所必需的。
03 建立因果联系:光遗传“拯救” Cdk5 缺失导致的恐惧缺陷
Cdk5 缺失导致的 M/T 细胞活性下降,是否就是恐惧行为减弱的直接原因?为了验证这一假设,研究者采用光遗传技术,在 Cdk5 缺陷小鼠中特异性地激活 M/T 细胞,并观察小鼠恐惧行为的变化 (图7A-C)。结果显示,光激活的 M/T 细胞能够显著逆转 Cdk5 缺失导致的恐惧反应缺陷,使小鼠在面对 nTMT 刺激时,其回避和僵硬行为显著提升(图7D-I)。这一结果完美建立了 M/T 细胞活性降低与 Cdk5 缺失导致的恐惧缺陷之间的因果联系,证明了嗅球中 M/T 细胞对先天恐惧的编码依赖于正常的 Cdk5 表达。
本研究从模式识别 - 探索机制 - 因果验证的逻辑中系统性地回答了嗅球中的 M/T 细胞如何编码由捕食者气味引发的不同强度的先天恐惧行为这一核心科学问题。除了巧妙的实验设计和多学科技术的融合外,一个不可或缺的基石,便是对动物复杂行为的精准、客观的量化分析能力 。这项工作不仅为理解先天恐惧的神经基础提供了全新的、更为精细的认知框架,也为探究与情绪障碍相关的神经环路功能异常提供了重要线索和新的治疗思路。
04 Bayone 助力科研
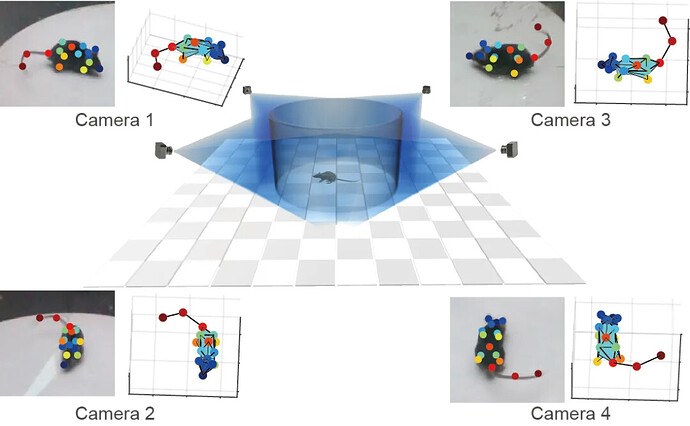
文章中助力研究者精准捕捉并量化小鼠逃避与僵硬行为的利器,正是一湾生命科技(BAYONE)的创新产品—— BehaviorAtlas 3D-AI 动物行为分析系统。它利用多视角深度摄像头和先进的 AI 算法,实现了对实验动物无标记的 3D 骨架动态追踪和无偏见的精细行为谱识别 ,并基于 3D 姿态和动态参数,将“主动回避”和“被动僵硬”这两种行为进行清晰的切割和量化,为后续与电生理信号的同步关联分析提供了高质量的行为学数据 。从焦虑、抑郁、自闭症等复杂精神疾病的动物模型评估,到神经退行性疾病的早期行为表型筛查,再到新药研发的药效评价, BehaviorAtlas 都能提供前所未有的深度和广度。我们的产品还在许多优秀的研究工作中得到验证,如果您希望深入了解其在动物行为研究中的应用,我们非常欢迎您进一步探索!
如果您对BehaviorAtlas 3D-AI 动物行为分析系统感兴趣,欢迎通过公众号私信或扫描下方的微信二维码联系我们,我们将竭诚为您提供更多信息和帮助。
参考文献:
————————————————
Xu H, Yuan H, Song H, et al. Multimode neural population coding of diverse innate fear response by mitral and tufted cells. Cell Rep. 2025;44(9):116255. doi:10.1016/j.celrep.2025.116255