该研究利用深度学习行为分析,证明了 “疼痛” 并非简单的反射,而是一种潜在的情感-动机状态,这种状态可以被 ACC 神经活动精确预测。基于此机制,研究团队开发了一种化学遗传学基因疗法,在慢性神经病理痛模型中有效保留了吗啡的镇痛效果,更重要的是,在实验周期内未出现耐受、成瘾以及呼吸抑制等副作用,这为精准疼痛管理提供了全新的策略。
疼痛并非单纯的伤害性输入,而是由脊髓和大脑回路塑造的一种融合感官辨别、情绪厌恶与动机驱动的复杂体验。当疼痛从急性保护信号转为慢性病理状态,其持久的情绪-动机驱动成为临床最大痛点——现有阿片类药物虽能减轻疼痛带来的 “不愉快感”,因其作用于广泛表达的分子靶点,也带来呼吸抑制、耐受与成瘾等严重副作用。因此,人类急需寻求更安全、更精准的治疗方法。
越来越多的研究表明,前扣带回皮层(Anterior Cingulate Cortex, ACC)是大脑中编码疼痛情感和动机维度的关键区域。临床研究表明,ACC 的神经活动与主观感知的 “疼痛不愉快感” 高度相关。顽固性疼痛患者接受扣带回切除术后,他们依然能感觉到疼痛的强度,但不再对此感到痛苦,这证明了疼痛的 “感觉” 与 “情感” 是可以分离的。因此,了解疼痛体验的情感和动机特征背后的神经回路和细胞类型对于推进慢性疼痛患者的精准治疗至关重要。
2026 年 1 月 7 日,宾夕法尼亚大学的 Gregory Corder 团队与卡内基梅隆大学的 Eric A. Yttri 团队在 Nature 发表的题为 “ Mimicking opioid analgesia in cortical pain circuits ” 研究论文中揭示:
ACC 中存在特定的 𝜇-阿片受体(MOR)阳性神经元集群,它们不仅是编码痛觉的 “情感-动机状态”,还是吗啡产生镇痛作用的关键靶点 。基于此,研究团队开发了一种生物启发式的化学遗传学基因疗法,利用合成的 𝜇-阿片受体启动子(MORp)特异性沉默 ACC 中的阿片敏感神经元。这种方法在慢性神经病理痛模型中有效保留了吗啡的镇痛效果,更重要的是,在实验周期内未出现耐受、成瘾以及呼吸抑制等副作用,这为精准疼痛管理提供了全新的策略。
疼痛模型
研究团队通过左后爪注射福尔马林和辣椒素建立小鼠急性疼痛模型,通过神经损伤建立小鼠慢性神经病理痛模型。
01 AI 行为解析“疼痛情感-动机状态”
目前临床前(动物)疼痛研究主要依赖反射性缩足反应(如 Von Frey 测试)。这些反射仅评估脊髓层面的诱发反应,无法捕捉到慢性痛患者最关心的持续性情感体验。即使是条件位置偏好等测试,也只能测量基于记忆的反应,而无法捕捉由自发性疼痛驱动的、动态的、即时的动机行为。
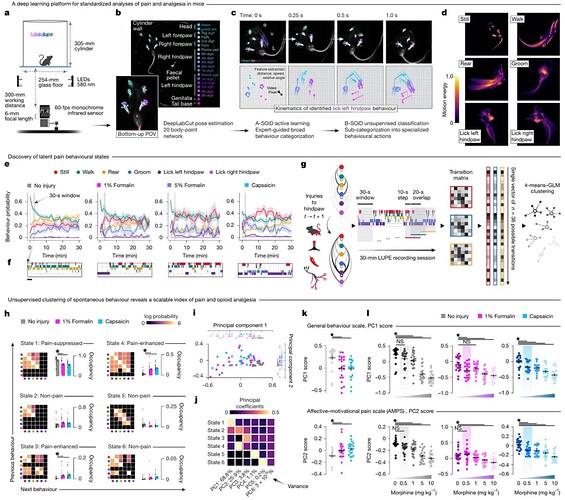
为了解决这一问题,研究团队开发了名为 LUPE (Light Automated Pain Evaluator) 的 AI 驱动行为分析平台。通过底部的高速红外摄像机记录小鼠,利用 DeepLabCut 追踪 20 个身体关键点。随后,结合 A-SOiD(半监督)和 B-SOiD(无监督)算法,将复杂的行为流分割为六种基本行为谱(图 1a-c):静止(Still)、行走(Walk)、直立(Rear)、理毛(Groom)、舔左后爪(Lick left)、舔右后爪(Lick right)。
在足部注射福尔马林或辣椒素后,小鼠并未表现出单一的刻板行为,而是行为模式发生了动态转变。通过计算 30 秒时间窗内的行为转移矩阵,并使用 k-means 聚类,识别出了 6 种宏观的“潜在行为状态”。其中,State 4 被定义为 “疼痛增强状态”,其特征是高概率的受伤左侧后爪舔舐行为。通过系统给药吗啡能够剂量依赖性地特异性抑制疼痛状态,表明该状态具有阿片敏感性(图 1h)。
为了简化分析,研究者对状态分布进行了主成分分析(PCA)。第一个主成分(PC1)主要反映了被损伤和大剂量吗啡破坏的基础活动水平,被称为一般行为量表,第二成分(PC2)对损伤和镇痛有双向反应——损伤使其升高,吗啡使其降低。因此,PC2 被定义为“情感-动机疼痛量表”(AMPS),成为衡量疼痛厌恶程度的客观量化指标(图 1i-l)。
02 ACC 神经动态追踪急性疼痛与镇痛过程
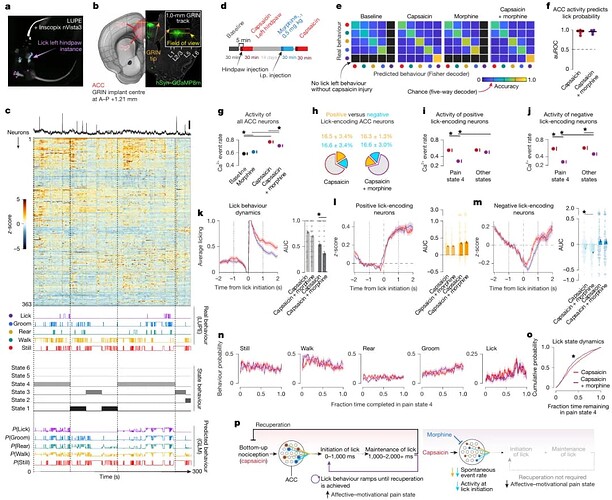
为了将 ACC 活动与吗啡敏感性疼痛行为联系起来,研究团队利用活体钙成像在 LUPE 系统中同步记录小鼠自由活动时的神经元钙信号,通过将神经活动与行为和潜在状态对齐,并拟合广义线性模型(GLM)来预测舔舐概率,识别出了一群特定的神经元——P lick 神经元(图 2a-f)。
这些 P lick 神经元被进一步细分为阳性(舔舐开始时兴奋)和阴性(舔舐开始时抑制)亚群,这些神经元亚群共同编码疼痛引起的动机性行为(图 2h-j)。吗啡处理并不影响整体神经活动,而是特异性地调节这些特定神经元在疼痛状态下的活动模式 ,破坏维持“疼痛状态”的神经动力学基础,从而发挥镇痛作用(图 2k-p)。
03 吗啡修复慢性痛导致的功能性神经环路损伤
在慢性神经病理痛(SNI模型)中,ACC 的编码机制是否发生改变?吗啡是否依然有效?
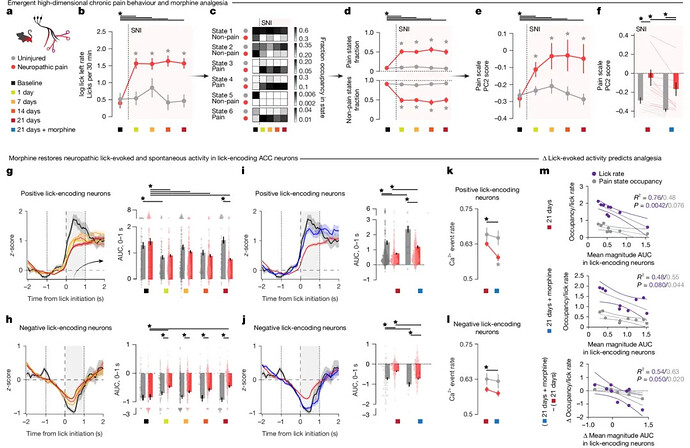
在 SNI 手术后 3 周内,小鼠表现出持续升高的 AMPS 评分和 “疼痛增强状态(State 4)” 占用率。单次吗啡注射(0.5 mg/kg)可显著逆转这些指标,说明该模型对阿片类药物敏感(图 3a-f)。
在慢性痛状态下,ACC 神经元对舔舐行为的编码能力下降。具体表现为,P lick 神经元在舔舐发生时的反应幅度变小(图 3g, h)。而在吗啡治疗后, P lick 神经元的反应幅度显著恢复到基线水平(图 3i, j)。此外,线性回归显示,舔舐诱发的神经活动幅度与舔舐频率和疼痛状态占用率呈正相关,吗啡引起的神经活动幅度增加预示着在疼痛状态下的行为和时间的减少(图 3m)。
04 基于阿片受体细胞类型的精准化学遗传学基因疗法
既证实了 ACC 中 MOR+ 神经元是关键靶点,能否绕过全身给药,通过基因工程手段精准调控这群细胞来实现镇痛?
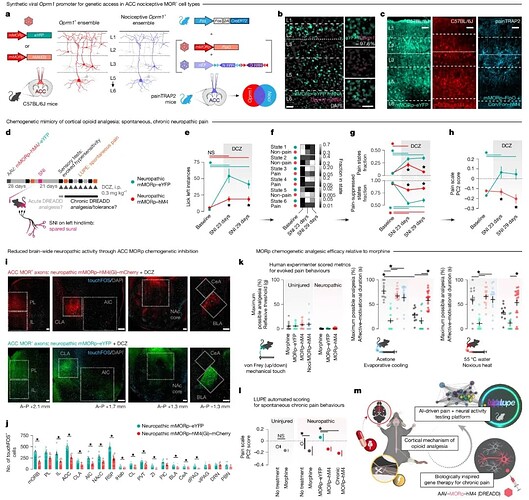
研究团队通过截取小鼠 prm1 基因上游 1.5kb 的调控序列,构建了 AAV-MORp 载体,通过给药靶向抑制 ACC 中的 MOR+ 神经元(图 4a-c)。在慢性神经病理痛(SNI)模型中,该疗法显著降低了小鼠的自发性疼痛行为和情感-动机疼痛评分(AMPS),且长期给药不产生耐受(图 4d-h)。全脑 FOS 成像显示,抑制 ACC MOR+ 神经元后,下游 14 个痛觉相关脑区的过度兴奋受到广泛抑制,这说明 ACC 是疼痛网络的关键 “枢纽”(图 4i-j)。
最具临床意义的是,该疗法完美实现了 “痛觉与痛苦” 的分离:它有效缓解了疼痛的情感厌恶成分,但完全保留了正常的机械性痛觉反射(Von Frey测试),这表明,基于 MORp 的化学遗传疗法可模拟吗啡的镇痛作用,在某些情况下,可能对慢性疼痛的情感 - 动机特征提供更优的疗效(图 4k-i)。
更关键的是,在实时位置偏好(RTPP)实验中,相比慢性痛小鼠,对 ACC MOR+ 神经元的光遗传抑制并没有改变正常小鼠在条件反射或回忆过程中的舱室偏好,表明慢性抑制 ACC MOR+ 神经元产生稳定的,状态依赖性镇痛,在正常情况下没有耐受或成瘾。
这些结果证明了该疗法在保留吗啡对情感性疼痛的强大镇痛效力的同时,避免了全身使用阿片类药物带来的耐受、成瘾和生理副作用。
这项工作将 AI 驱动的行为解码与神经科学相关联,它不仅在理论上阐明了 ACC 阿片环路在疼痛情感维度的核心作用,并以自主构建的 LUPE 深度学习平台量化自发痛行为状态,建立可复现的 AMPS 情绪痛指标。在此基础上,团队设计 AAV-MORp-hM4Di 化学遗传疗法,实现长时程、无耐受、非成瘾的类吗啡镇痛,为替代系统性阿片提供可直接临床转化的精准干预方案。
05 Bayone产品介绍
还在为 “自发行为” 找不到客观标尺?还在因人工标注耗时、主观、不可复现而头疼?还在为三维精细姿态、毫秒级动态与神经同步记录无法兼得而犯难?
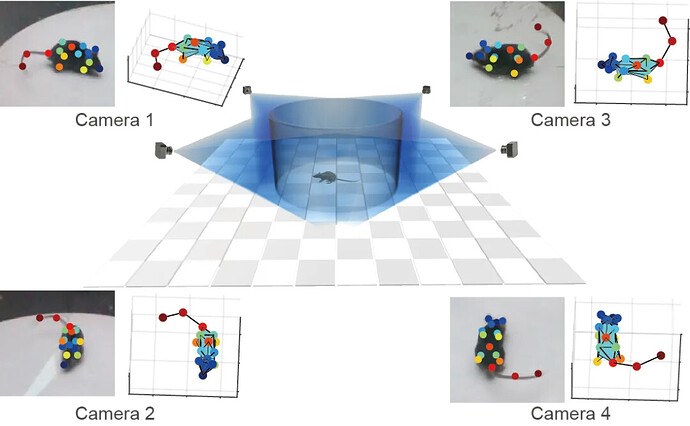
一湾生命科技(BAYONE)的创新产品—— BehaviorAtlas 3D-AI 动物行为分析系统,依托多视角深度摄像头和先进的 AI 算法,实现了对实验动物无标记的 3D 骨架动态追踪和无偏见的精细行为谱识别。从焦虑、抑郁、自闭症等复杂精神疾病的动物模型评估,到神经退行性疾病的早期行为表型筛查,再到新药研发的药效评价,BehaviorAtlas 都能提供前所未有的深度和广度。我们的产品还在许多优秀的研究工作中得到验证,如果您希望深入了解其在动物行为研究中的应用,我们非常欢迎您进一步探索!
为了帮助您获取更多信息,我们提供了便捷的联系方式。您可以通过公众号私信与我们交流,或者直接扫描下方的微信二维码,我们的专业团队将竭诚为您提供更多信息和帮助。
参考文献:
————————————————
Oswell, C.S., Rogers, S.A., James, J.G. et al. Mimicking opioid analgesia in cortical pain circuits. Nature (2026). Mimicking opioid analgesia in cortical pain circuits | Nature