2026 年 2 月 11 日, 深圳先进院脑所的王立平团队在 Neuron 上发表研究论文,研究通过电生理学记录、单细胞转录组学、基因编辑 / 病毒操控、 3D 精细行为学等技术,层层解析了骨钙素(Osteocalcin, OCN)调控共释放神经元兴奋性、促进快速逃逸反应的神经回路机制,这一发现为骨-脑代谢轴调控生存行为的研究提供了新视角。该研究论文应用了一湾生命科技(BAYONE)自主研发的 3D-AI 小鼠行为分析系统,为正常小鼠和 OCN 敲除小鼠的精细化行为研究提供了重要工具支撑。
快速逃离视觉威胁是动物生存的基本能力,依赖于神经回路的快速激活。王立平研究团队早期研究揭示了大脑腹侧被盖区(VTA)GABA 能神经元是对模拟捕食者逼近刺激(Looming stimuli)的视觉逃逸反应的关键信息中继站,接收来自上丘的视觉威胁信号,并传递给恐惧中枢杏仁核,引发逃逸。(点击查看往期相关文献解读)然而,这些 VTA 特定神经元的兴奋性如何被精确调控,建立高度警觉的预备状态(Permissive state)以实现快速、即时反应的细节仍未可知。
穿越血脑屏障的外周来源分子对于调节防御行为至关重要。OCN 是仅由骨组织分泌的激素,可穿过血脑屏障调控中枢神经功能,此前发现其参与应激诱导的防御行为,但尚未发现其与视觉逃逸反应的关联,且其在中枢的分子作用靶点与通路未知。
2026 年 2 月 11 日,中国科学院深圳先进院脑所的王立平研究团队在 Neuron 发表题为 “A bone-derived hormone permits rapid visual escape via GPR37 receptor in a subpopulation of VTA GABAergic neurons” 的研究论文。该研究首次揭示 OCN 这种骨源性激素,通过激活 VTA GABA 能神经元的一个亚群中的 GPR37 受体,作为快速视觉逃逸的关键调节因子。OCN-GPR37 通路通过 cAMP-THIK-1 这一非经典信号通路迅速增强神经元兴奋性,进而驱动在急性天敌应激的快速逃逸反应。这些发现揭示了一种新的相互作用,即骨骼系统调节中脑神经元特性以协调生存行为。
01 关键因子
OCN 和 GPR37 是快速视觉逃逸反应的必要因子
首先为了探究 OCN 在视觉逃逸行为中的潜在作用,研究比较了 Looming 刺激下年轻(3 月龄)和老年(14 月龄)野生型(WT)小鼠的防御反应(图1A,B)。结果表明,老年鼠相比年轻鼠,血清中的 OCN 水平显著下调(图1C),且表现出显著延迟的反应潜伏期和更长的返回巢穴时间 (图1D),而腹腔注射 OCN 可完全恢复老年小鼠的正常防御行为(图1E)。此外,Looming 刺激这一单一因素可使小鼠血清 OCN 水平急剧升高并至少维持 30 分钟(图 1F)。这些结果证实了 OCN 是视觉逃逸反应的关键介导因子。
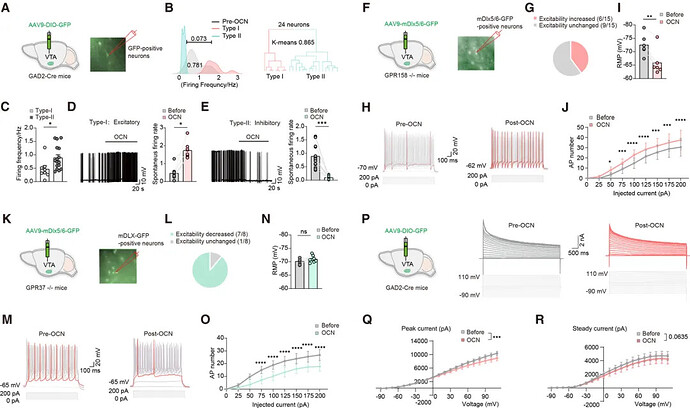
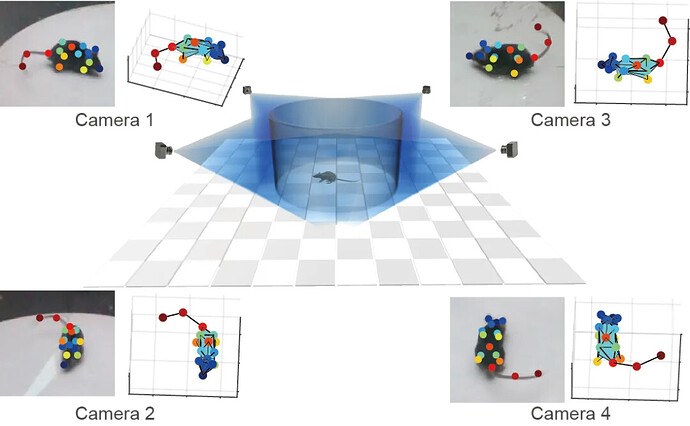
值得一提的是,研究应用了一湾生命科技(BAYONE)自主研发的 3D-AI 小鼠行为分析系统监测小鼠的自发性行为(图2A)。结果显示,WT 小鼠与 OCN 敲除小鼠在实验区域中央的停留时间、运动速度,且二者在各类自发性行为中的时间占比也无明显不同(图2B-D)。这表明 OCN 特异性调控视觉逃逸反应,而非影响小鼠的自发性行为或焦虑相关行为。
为了进一步明确 OCN 在视觉逃逸行为中的作用靶点,研究通过实验证实了 OCN 敲除小鼠、GPR37 敲除小鼠均出现逃逸反应缺陷,而 GPR158(另一候选受体)敲除小鼠行为无异常(图1G),说明 OCN 主要通过 GPR37 介导视觉逃逸反应。
02 作用靶点
OCN 激活 VTA 脑区中特定的 GABA 能/谷氨酸能神经元亚群上的 GPR37 受体
已知 VTA 区是介导 Looming 刺激诱导的防御反应的核心枢纽,研究验证了 VTA 区内的 OCN 信号是否能挽救 OCN 敲除小鼠的防御行为缺陷,结果显示:向 OCN 敲除小鼠的 VTA 区微注射 OCN,可恢复其逃逸行为(图2A-C);与之相似的是,恢复 GPR37 敲除小鼠 VTA 区的该受体表达,也可恢复小鼠的快速逃逸反应(图2D-F);但是向 GPR37 敲除小鼠的 VTA 区注射 OCN 则无法挽救其受损的防御行为(图2G,H)。这些结果证实了 VTA 是 OCN 发挥作用的关键靶点,且其功能依赖 GPR37。
研究通过特异性受体敲除实验进一步明确了 VTA 区中介导 OCN-GPR37 信号通路控视觉逃逸反应的神经元类型,实验结果显示:特异性敲除 VTA 区多巴胺能神经元的 GPR37,不会影响小鼠逃逸行为(图3A-D);而特异性敲除 VTA 区 GABA 能神经元或谷氨酸能神经元的 GPR37,均会导致小鼠逃逸反应延迟(图3E-H)。这些结果证实了 OCN 通过调控 VTA 区这两类神经元的 GPR37 介导逃逸行为。
03 神经回路
OCN 调控 VTA 的 GABA 能神经元分为两个功能不同的兴奋性亚群
研究通过膜片钳技术进一步探究 OCN 对 VTA GABA 能神经元的调控作用,结果显示:基础状态下,VTA 的 GABA 能神经元兴奋性无明显亚群差异;OCN 处理后,该类神经元被分为 Ⅰ 型(兴奋性增强)和Ⅱ 型(兴奋性降低) 两个亚群(图5A,B)。基础状态下,Ⅰ 型神经元基础自发放电率显著低于 Ⅱ 型,其余膜电生理参数无差异;OCN 处理后,Ⅰ 型放电率显著升高,Ⅱ 型显著降低,且该变化不依赖突触传递(图5C-E)。并且发现调控存在受体特异性介导,GPR37 介导兴奋性增强,GPR158 介导兴奋性降低(图5F-O)。此外研究结果进一步证实了 OCN 通过调控钾电流来调节神经元的兴奋性(图5P-R)。
OCN 的下游关键钾通道:THIK-1(Kcnk13) 与 GIRK1(Kcnj3)
为了进一步探究是哪种钾离子通道参与了 VTA GABA 能神经元的调控。研究对 VTA 组织进行单细胞测序发现:VTA 中 70% 的 GABA 能神经元为 GABA-谷氨酸共释放神经元,是 OCN 的主要作用靶点(图6A,B)。研究验证了GPR37 与 GPR158 分别和 THIK-1 通道以及 GIRK1 通道存在较强的相关性,且这两个钾通道是调控神经元兴奋性的核心靶点(图6C,D)。在细胞表达水平上,GPR37 与 THIK1(Kcnk13)共同表达于GABA-谷氨酸共释放 I 型神经元中,而 GPR158 与 GIRK1(Kcnj3)则在 II 型神经元中共同表达(图6H)。
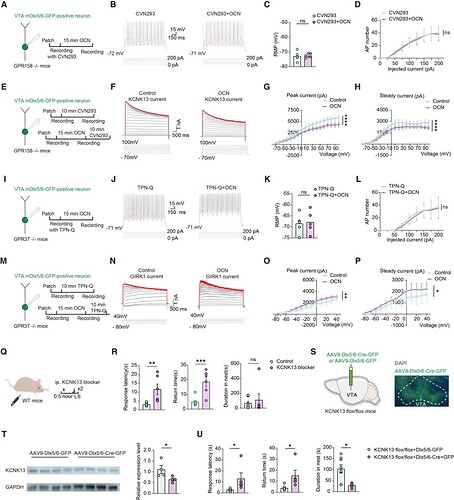
研究为进一步证实 OCN,钾通道与神经元兴奋性之间存在受体依赖性的关联,开展了相关功能验证实验。在功能验证水平上,研究证明了 OCN 可显著抑制 VTA GABA 能神经元的总钾电流;特异性阻断 THIK-1(CVN293)可模拟OCN 的作用,增强神经元兴奋性;阻断 GIRK1(TPN-Q)则抑制其兴奋性(图7)。
OCN 调控视觉逃逸反应的核心分子通路
研究通过特异性表达探针技术,发现 Looming 刺激可诱导 WT 小鼠 VTA GABA 能神经元的环腺苷酸(cAMP)显著降低、Ca²⁺ 升高,而 OCN 敲除小鼠的均无变化(图8A-H)。而 GPR37 敲除小鼠的补充实验结果显示,与 WT 小鼠相比, GPR37 敲除小鼠的 cAMP 显著升高,而通过对其注射 cAMP 阻断剂能恢复逃逸行为(图8I-K),证实了 cAMP 降低是小鼠视觉逃逸反应的必要条件。
综上,研究阐明了分子机制:OCN 激活 GPR37 后,通过非经典 Gi 通路降低细胞内的 cAMP 水平,进而抑制 THIK-1 钾通道,最终增强 VTA 区 GABA 能神经元的兴奋性,使小鼠在面临视觉威胁时能做出快速的逃逸反应(图 8L)。 研究明确了 GPR37 在调控 cAMP 信号和神经元兴奋性、介导机体适应性行为中的关键作用。
04 总结
本研究的核心发现是,骨骼分泌的 OCN 是一种关键的骨源性激素,通过激活 VTA 中特定的 GABA 能以及谷氨酸能神经元亚群上的 GPR37 受体,触发 OCN-GPR37-cAMP-THIK-1 信号通路,进而能够促进快速视觉逃逸。 这项工作突出了骨骼系统如何通过其内分泌功能,调节 VTA 神经元的特性,从而协调对生存至关重要的行为。它连接了代谢、神经科学和生理学,为理解骨-脑轴的功能增添了新的维度,并为探索骨质疏松相关抑郁症和神经退行性疾病等疾病中的代谢干预开辟了新途径。
05 Bayone 助力科研
该研究论文应用了一湾生命科技(BAYONE)自主研发的 3D-AI 小鼠行为分析系统,为 OCN 敲除小鼠行为的精细化研究提供了重要工具支撑。 一湾生命科技致力于通过 AI 技术,为脑科学及脑疾病研究等领域提供新一代更高效、更精准的仪器、软件、服务和标准。一湾生命科技专注于推动 AI 精细行为学技术在神经疾病模型的研究中发现新的生物标志物、表型鉴定及愈后评估等方面的应用。如果您对这一技术感兴趣,欢迎了解更多关于 BehaviorAtlas 3D-AI 动物行为分析系统 的信息!
BehaviorAtlas 3D-AI 动物行为分析系统是国内首家3D-AI精细行为学分析系统,可以在三维层面分析动物的精细行为;追踪16+个身体点,实现行为全面量化;提取40+种行为亚型,包括嗅探、梳理、跳跃等行为;计算100+种参数,捕捉动物行为的每一个细节;输出专业级可视化图表,满足SCI论文发表要求。 目前,BehaviorAtlas 3D-AI 动物行为分析系统已经在大、小鼠、非人灵长类动物、犬类等模式动物上,针对自闭症、帕金森症、抑郁症、老年痴呆、脑出血等疾病模型以及精神类药物筛选上进行了多种应用。在此,我们也感谢 BehaviorAtlas 的用户对我们系统的关注和支持,希望 BehaviorAtlas 能够帮助更多的科研人员去解答生命科学中的难题。如果您希望深入了解其在动物行为研究中的应用,我们非常欢迎您进一步探索!
如果您对BehaviorAtlas 3D-AI 动物行为分析系统感兴趣,欢迎通过公众号私信或扫描下方的微信二维码联系我们,我们将竭诚为您提供更多信息和帮助。
参考文献:
————————————————
Xuemei Liu#, Shuaiyu Wang#, Juan Lai#, Xiang Gao, Lina Wang, Bo Feng, Liang Yang, Zhengjiang Qian, Ruotian Jiang, Jun Chu, Liming Tan, Xiang Li*,and Liping Wang*. A bone-derived hormone permits rapid visual escape via GPR37 receptor in a subpopulation of VTA GABAergic neurons. Neuron . (2026). ISSN 0896-6273. Redirecting.