脊髓损伤(SCI)后,神经元为什么会大量死亡?
该研究揭示了一个关键机制:过度的内质网-线粒体接触(ERMCSs) 。硬脂酰辅酶A 去饱和酶1(SCD1)缺乏是 ERMCS 异常扩张背后的驱动力,导致单不饱和脂肪酸(MUFAs)减少,进而诱发脂质过氧化增加和神经元铁死亡。相反,SCD1 过表达可以逆转这些影响。研究者发现核受体 LXRα 是 SCD1 的上游调控者。通过药物激活 LXRα 或 基因过表达 SCD1,可以恢复 MUFA 合成,解开过度的 ER-线粒体接触,抑制铁死亡。最重要的是,借助一湾生命 AI 小鼠运动功能分析系统,发现这种干预显著恢复了瘫痪小鼠的运动功能!
脊髓损伤(SCI)会导致脊髓组织的大量损伤,目前尚无安全有效的修复策略。因此,阐明 SCI 后神经元死亡的分子机制,寻找可干预的治疗靶点,是神经科学领域的紧迫任务。
SCI 的病理过程不仅包含原发性机械损伤,更重要的是随后发生的继发性损伤(Secondary Injury)。在这一阶段,微环境中的血管破裂、红细胞溶解导致铁过载,同时伴随活性氧(ROS)爆发,引发神经元的铁死亡(Ferroptosis)。铁死亡是一种铁依赖性的、由脂质过氧化驱动的调节性细胞死亡,已被证实是 SCI 后早期神经元丢失的主要原因。
既往研究发现,铁死亡的发生并非孤立事件,而是依赖于细胞器之间的通讯。特别是内质网-线粒体接触位点(ER-Mitochondria Contact Sites, ERMCSs),在生理状态下负责脂质交换和信号传递。然而,在病理应激下,过度的 ERMCSs 形成会充当“脂质过氧化物”的传输通道,将内质网产生的过氧化磷脂传递给线粒体,从而直接触发线粒体损伤和铁死亡。
神经元细胞膜富含多不饱和脂肪酸(PUFAs),这使得它们对脂质过氧化高度敏感。相比之下,单不饱和脂肪酸(MUFAs)具有抗氧化特性,能够通过竞争性替代磷脂中的 PUFAs 来抑制铁死亡。
为了阐明病理因素的关联以及分子机制,2026 年 2 月 10 日,中山大学附属第三医院刘斌、戎利民、庞卯、姚森誉团队在 Research 发表的题为 “ LXRα/SCD1-Mediated Endoplasmic Reticulum-Mitochondria Crosstalk in Inhibiting Neuronal Ferroptosis after Spinal Cord Injury ” 的研究中揭示:
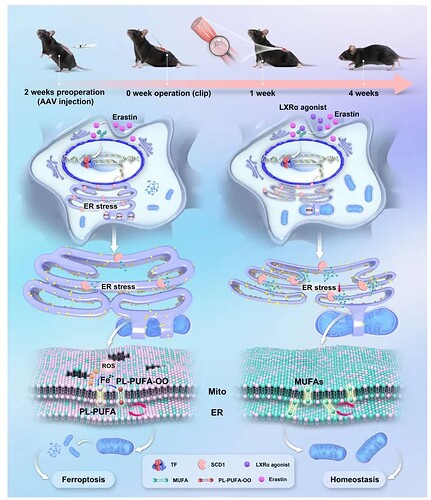
SCI 导致神经元内 SCD1 下调,这种减少驱动了 ERMCSs 的异常扩张,进而导致脂质过氧化增强和神经元铁死亡。研究发现,在机制上,转录因子肝 X 受体 α(LXRα)通过直接激活 SCD1 的转录,促使 MUFA 的富集,增强细胞的抗氧化能力,从而抑制铁死亡的进程。最为关键的是,研究者通过 LXRα 激动剂或过表达 SCD1 在小鼠模型中显著恢复了下行神经传导和运动功能。 综上所述,该研究确立了 LXRα–SCD1 通路 作为一个全新的、可成药的治疗靶点,能够通过调节依赖于 ERMCS 的脂质交换动力学来减少神经元丢失并改善功能恢复,揭示了中枢神经系统创伤后具有前景的治疗靶点。
01 LXRα-SCD1 通路在维持脂质稳态和抵抗铁死亡中的作用
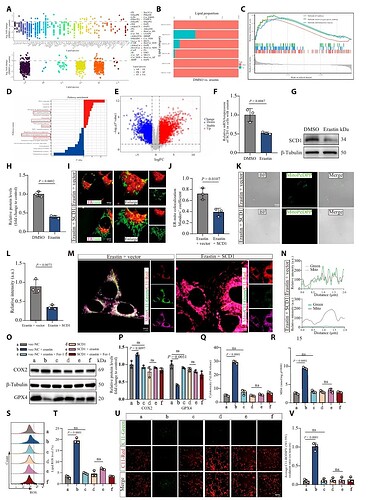
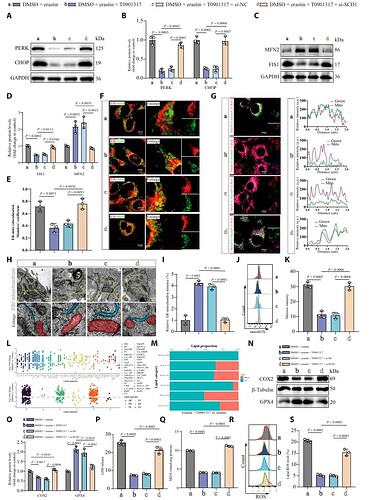
为了研究 SCI 后神经元铁死亡背后的分子机制,研究者通过分析 HT22 细胞在 Erastin(铁死亡诱导剂)处理后的转录组数据,发现 SCD1 显著下调(图1 F-G)。SCD1 负责合成单不饱和脂肪酸(MUFAs),其缺乏导致脂质代谢失衡,同时伴随包括 ROS、未折叠蛋白反应和 p53 信号在内的氧化应激通路激活(图 1A-E)。相反,恢复 SCD1 表达能有效保护线粒体功能,减轻神经元铁死亡(图1 I-V)。
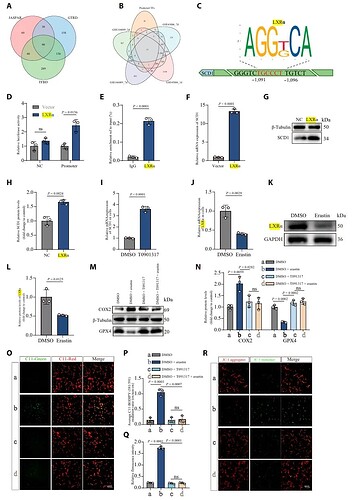
进一步的转录因子预测与生化实验结合发现,LXRα 是直接结合 SCD1 启动子并激活其转录的关键因子(图2 A-H)。LXRα 通过直接上调 SCD1 表达,进而减轻脂质过氧化和铁死亡的进程(图2 I-R)。此外,LXRα 敲低会加剧细胞铁死亡。这些发现明确了 LXRα-SCD1 通路在维持脂质稳态和抵抗铁死亡中的重要作用。
02 SCD1 缺失导致内质网和线粒体接触(ERMCS)增加
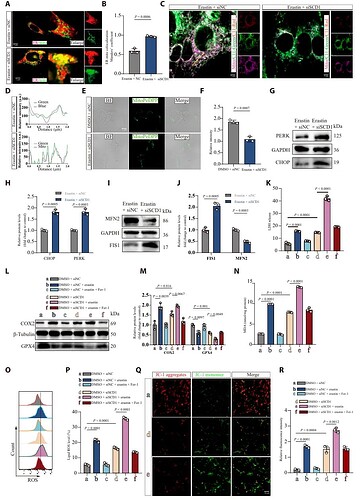
为了确认 LXRα-SCD1 通路的作用, 研究者通过共聚焦成像和透射电镜观察 SCI 后神经元的亚细胞特征,发现 SCI 显著增加了 ERMCS 的形成。同时,SCD1 的缺失会导致 ERMCS 的异常扩展(图3 A-F)。这种 “过度接触” 使脂质过氧化物大量从内质网转运到线粒体,进而引发线粒体损伤和铁死亡(图3 G-R)。
为了确认 LXRα-SCD1 通路是否可以作为 SCI 潜在治疗靶点,研究者在 SCI 小鼠模型中进行干预实验。实验分为治疗组(AAV-SCD1 过表达或给予 LXRα 激动剂 T0901317)、SCD1 敲低组 和对照组。结果显示,治疗组神经元的内质网-线粒体距离恢复正常,线粒体嵴结构完整(图4 A-D),然而,当 SCD1 被沉默,T0901317 的保护作用显著削弱。类似地,体外实验也验证了这一结果,同时伴随 MUFA 水平恢复,脂质过氧化和铁死亡被显著抑制 (图5)。
这些结果表明 LXRα 的神经保护作用依赖于 SCD1 介导的脂质重塑,LXRα-SCD1 通路通过维持 ERMCS 稳态、减少氧化应激和限制铁死亡信号传导,从而保护 SCI 后的神经元完整性。
03 干预策略:LXRα 激动剂/ SCD1 过表达恢复 SCI 小鼠运动功能
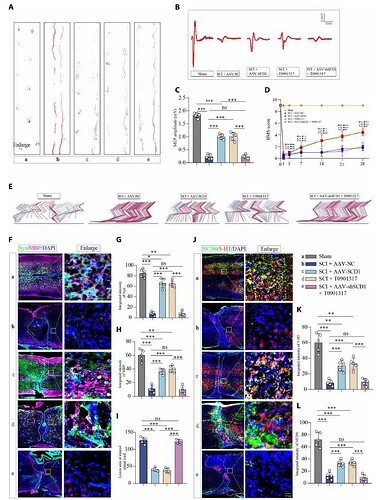
为了进一步评估该干预策略能否显著恢复 SCI 小鼠的运动功能,研究者进行了行为学评分和电生理实验。后肢足迹分析显示,治疗组小鼠步态显著改善,展现出清晰、规律的后肢脚印,步幅(Stride length)和步宽显著改善(图6 A)。电位检测(MEP)显示治疗组小鼠的 MEP 波幅显著回升、潜伏期缩短(图6 B-C)。
此外,Basso 小鼠量表(BMS)评分和步态运动学也证实了治疗组小鼠的运动改善。治疗组小鼠在术后 28 天的 BMS 评分达到 5-6 分区间,而对照组仅为 2-3 分,且治疗组小鼠恢复了典型的周期性摆动相(Swing phase),即后肢能够完成 “抬起-前摆-着地” 的完整循环,轨迹更接近正常小鼠,而非损伤组的拖地滑行(图6 D-E)。
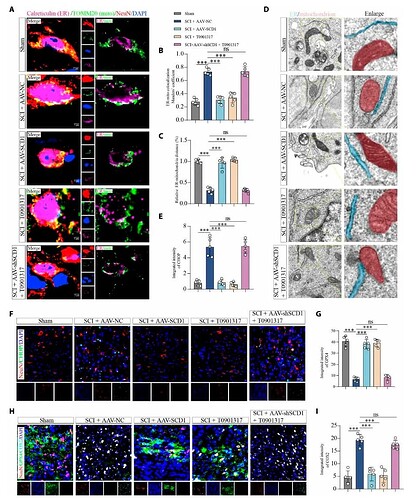
更重要的是,免疫荧光显示,治疗组脊髓病灶区域保留了更多的突触蛋白(Synapsin)、髓鞘碱性蛋白(MBP)以及 5-羟色胺能神经纤维(5-HT),表明轴突和髓鞘的完整性得到了改善(图6 F-L)。然而,这些保护作用在 SCD1 下调的情况下显著削弱。
这些结果表明 LXRα-SCD1 治疗策略的显著有效性,不仅恢复 MUFA 的合成和 内质网-线粒体的正常接触,阻断了铁死亡进程,更在小鼠模型中显著恢复了下行神经传导和运动功能。
总之,本研究全面论证了 SCD1 在 SCI 中的神经保护作用,并确定 LXRα–SCD1 轴是调节脂质代谢和内质网-线粒体互作的关键调控通路。通过缓解氧化应激和铁死亡,该轴有助于改善功能恢复。总的来说,这些发现不仅增强了我们对 SCI 发病机制的理解,而且揭示了用于神经保护和修复的新型治疗靶点。
该研究论文应用了一湾生命科技(BAYONE)自主研发的 BehaviorAtlas AI 小鼠运动功能分析系统,为脊髓损伤后运动功能修复的精细化评估提供了关键工具支撑。一湾生命科技致力于通过 AI 技术,为脑科学、脊髓损伤与神经修复等领域提供新一代更高效、更精准的仪器、软件、服务和标准。一湾生命科技专注于推动 AI 精细行为学技术在中枢神经系统损伤、神经退行性疾病、运动障碍模型的研究中发现新的生物标志物、表型鉴定及愈后评估等方面的应用。如果您对这一技术感兴趣,或者需要进一步了解如何通过专业步态分析软件,复现类似研究中的脊髓损伤运动功能评估范式,或针对特定步态、运动行为实验定制分析方案,欢迎了解更多关于 BehaviorAtlas 3D-AI 小鼠运动功能分析系统 的信息!
如果您对 BehaviorAtlas 3D-AI 小鼠运动功能分析系统感兴趣,欢迎通过公众号私信或扫描下方的微信二维码联系我们,我们将竭诚为您提供更多信息和帮助。
参考文献:
————————————————
Jiang P, Luo Y, Huang D, He J, Li H, Xiao L, Yao S, Pang M, Rong L, Liu B. LXRα/SCD1-Mediated Endoplasmic Reticulum-Mitochondria Crosstalk in Inhibiting Neuronal Ferroptosis after Spinal Cord Injury. Research . 2026;9:1077. DOI: 10.34133/research.1077