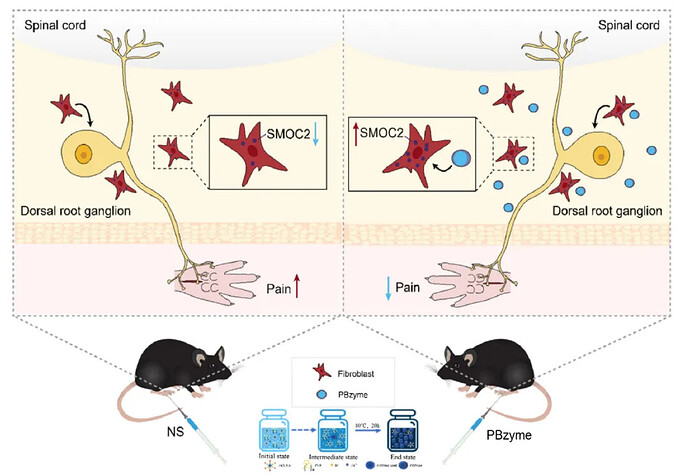
近日,上交大顾希垚 / 蔡晓军 / 俞卫锋 / 张松团队通过 BehaviorAtlas 3D-AI 动物行为分析系统,精准量化了 PBzymes 对术后小鼠擦脸、僵直等核心自发性疼痛样行为的缓解作用,同时捕捉到其对疼痛伴随的扑跃、攀爬、弓背等焦虑样行为的改善效应,突破了传统诱发性痛阈检测仅能反映反射性痛觉应答的局限,实现了术后疼痛多维度病理表型的全自动化、无偏精细化量化评估,为术后疼痛的非阿片类治疗提供了全新理论认识,也为纳米酶调控内源性镇痛通路的疼痛干预策略奠定了重要转化基础。一湾生命科技 BehaviorAtlas 3D-AI 动物行为分析系统为本论文中的行为学分析提供了强有力的技术支持!
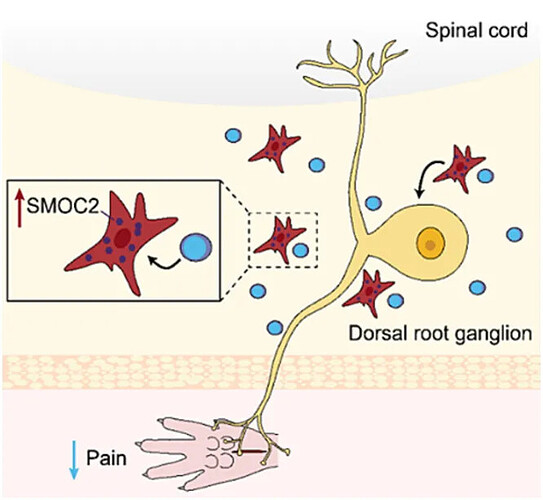
术后疼痛是临床外科领域最常见的急性疼痛问题,也是导致患者术后康复延迟、睡眠障碍,甚至进展为慢性疼痛的重要危险因素。目前临床术后镇痛仍以阿片类药物为核心方案,但该类药物易引发成瘾、耐受、呼吸抑制、便秘等一系列不良反应,安全、非成瘾、外周靶向的新型镇痛策略已成为临床与科研的迫切需求。背根神经节(dorsal root ganglion, DRG)作为伤害性感觉信号传递的 “第一门户”,其内部感觉神经元异常兴奋、微环境失衡是术后机械性痛觉超敏发生与维持的关键结构基础。近年来研究证实,DRG 内成纤维细胞并非单纯结构支持细胞,而是通过分泌多种细胞外基质蛋白参与疼痛调控,其中分泌性模块化钙结合蛋白 2(secreted modular calcium-binding protein 2, SMOC2)可特异性抑制机械性痛觉信号传导,成为极具潜力的内源性镇痛靶点。然而,如何在不使用外源性药物的前提下,安全、原位激活机体自身 SMOC2 镇痛通路,实现 “内源性镇痛”,至今仍缺乏有效解决方案。普鲁士蓝(Prussian blue, PB)是经美国 FDA 批准的临床解毒剂,体内应用安全性明确,已在放射性物质与重金属中毒救治中长期使用。近年来,以普鲁士蓝为基础制备的纳米酶(PBzymes) 因其良好生物相容性、多重类酶活性与微环境调控能力,在神经保护、抗炎、抗氧化应激等领域受到广泛关注。然而,PBzymes 是否可作用于背根神经节(DRG)微环境、调控内源性镇痛分子以缓解术后疼痛,以及具体分子机制尚未被阐明。
2026 年 2 月 18 日,上海交通大学医学院附属仁济医院顾希垚/俞卫锋/张松和附属第六人民医院蔡晓军团队在 Journal of Advanced Research 上在线发表了题为 “Prussian blue nanozymes alleviate postoperative pain via upregulating endogenous SMOC2 secretion in dorsal root ganglion fibroblasts” 的研究论文,该研究首次提出并证实 “内源性镇痛” 全新机制,明确普鲁士蓝纳米酶可通过上调 DRG 成纤维细胞 SMOC2 分泌,抑制神经元异常兴奋,从而持续、选择性缓解术后机械性痛觉超敏。研究团队结合 3D 运动捕捉 AI 行为学分析系统,对小鼠术后疼痛相关自发行为、疼痛伴随焦虑样行为进行无偏、精细化、全自动量化评估,客观、全面地验证了 PBzymes 对术后疼痛的改善效应,为术后疼痛非阿片类神经调控治疗提供了全新分子靶点、全新作用机制和重要临床转化基础。
01 普鲁士蓝纳米酶的合成与表征
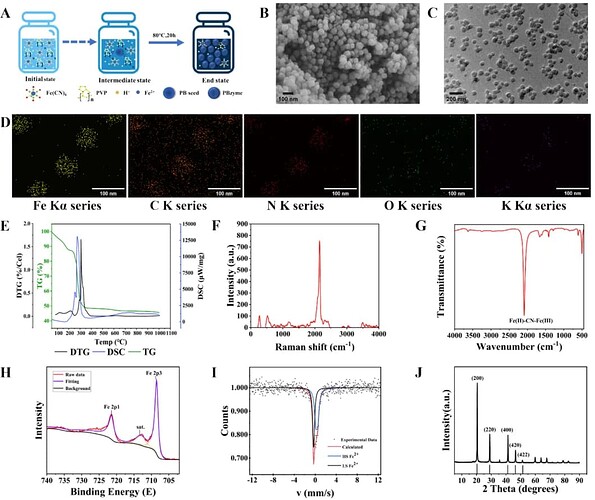
普鲁士蓝(PBzymes,PB)是美国 FDA 正式批准的临床解毒剂,具备抗氧化、抗炎、维持组织微环境稳态等多重生物活性,在神经保护与组织修复领域已展现出良好应用潜力。但普通普鲁士蓝为微米级颗粒,存在细胞摄取效率低、组织渗透性差、生物活性发挥受限等问题。将其制备为纳米级普鲁士蓝(PBzymes),能够优化颗粒尺寸与表面特性,提升细胞摄取与组织滞留能力,并增强其类酶催化活性,是在体干预研究的理想材料。基于此,研究者通过改良水热法成功合成普鲁士蓝纳米酶(PBzymes),并对其理化性质进行系统表征(图 2A)。
扫描电镜与透射电镜结果显示,所制备的 PBzymes 呈球形、大小均一、分散性优异(图 2B–C)。元素 mapping 证实 Fe、K、C、N、O 在颗粒内部分布均匀(图 2D)。热重分析、拉曼光谱、红外光谱、X 射线光电子能谱、穆斯堡尔谱与 X 射线衍射结果共同证明,PBzymes 具有标准普鲁士蓝晶体结构,理化性质稳定、结晶度良好(图 2E–J)。上述结果表明,本研究成功合成结构均一、性质稳定、符合生物医学应用要求的 PBzymes,为后续体内外实验奠定材料基础。
02 PBzymes 特异性缓解术后机械性痛觉超敏
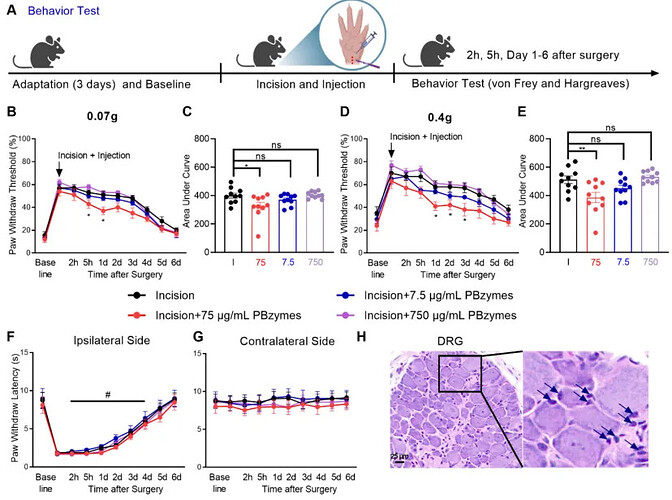
基于已完成表征的 PBzymes 材料,研究者构建小鼠足底切口术后疼痛模型,通过单次外周注射不同浓度 PBzymes,评估其对术后疼痛行为的调控作用(图 3A)。von Frey 机械痛实验结果显示,75 μg/mL PBzymes 可显著、持续地缓解术后机械性痛觉超敏,在 0.07 g 与 0.4 g 两种刺激强度下均明显降低缩足频率,曲线下面积分析进一步证实该剂量具有稳定镇痛效果,效应可持续至术后 6 天(图 3B–E);7.5 μg/mL 与 750 μg/mL PBzymes 未产生显著镇痛作用,整体呈钟形剂量–效应关系。激光热痛实验显示,PBzymes 未改变热痛觉过敏表型,提示其镇痛作用具有机械痛模态选择性,不影响热痛传导(图 3F–G)。伊红染色结果显示,PBzymes 可经坐骨神经转运并富集于 DRG 区域,为其靶向 DRG 发挥作用提供了组织学依据(图 3H)。
03 3D 行为分析证实 PBzymes 改善疼痛相关异常行为
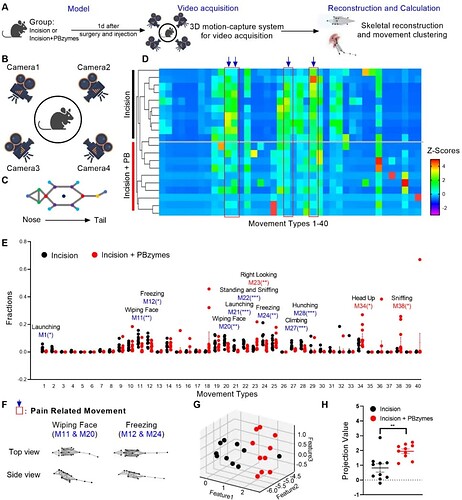
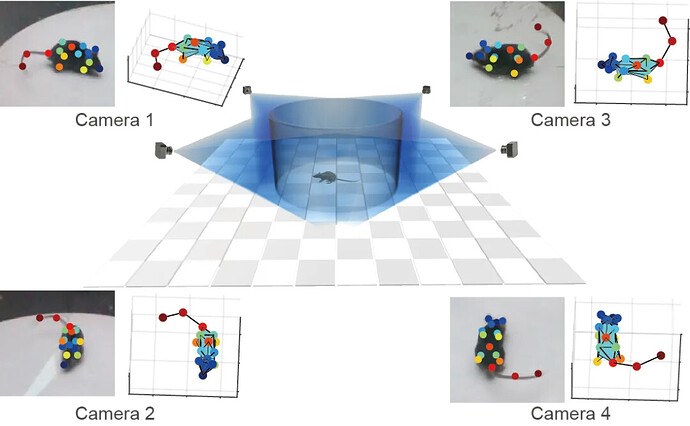
为更全面、客观地评估自发性疼痛与情绪相关行为改变,研究者采用 BehaviorAtlas 3D-AI 动物行为分析系统,对术后小鼠进行无偏、精细化行为量化(图 4A)。该系统通过四机位相机采集 16 个解剖学锚点轨迹,完成三维重建与行为聚类分析(图 4B–C),共识别 40 种运动类型(图 4D)。结果显示,与切口组相比,PBzymes 处理组小鼠擦脸、僵直等疼痛样行为占比显著降低,扑跃、攀爬、弓背等焦虑样行为也明显减少(图 4E–F)。降维分析与 X 轴投影进一步证实,PBzymes 组运动模式更接近正常生理状态,从全行为谱层面验证其对术后疼痛相关异常行为的改善作用(图 4G–H)。
04 转录组学揭示 PBzymes 调控 DRG 细胞外基质通路
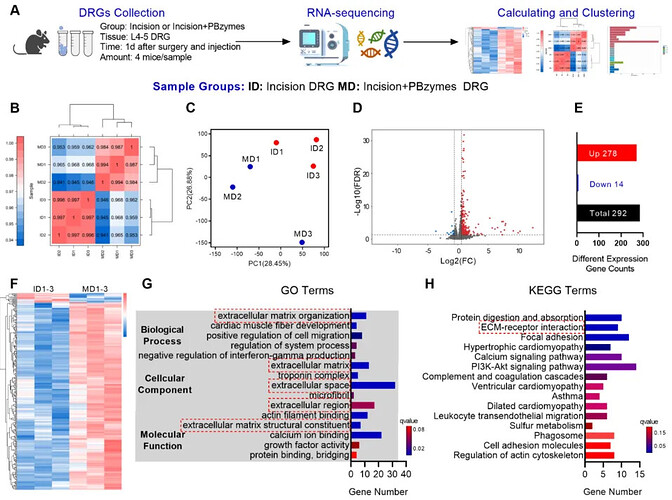
为挖掘 PBzymes 镇痛的分子机制,研究者对术后 1 天小鼠 L4–L5 DRG 组织进行转录组测序(图 5A)。样本相关性与主成分分析显示,切口组与 PBzymes 处理组基因表达谱存在显著差异,提示 PBzymes 可显著调控 DRG 基因表达(图 5B–C)。分析共鉴定到 292 个差异基因,GO 与 KEGG 富集分析一致表明,差异基因高度富集于细胞外基质(ECM)相关通路,提示 PBzymes 可能通过调节 DRG 微环境发挥作用(图 5G–H)。
05 PBzymes 显著上调 DRG 成纤维细胞 SMOC2 表达
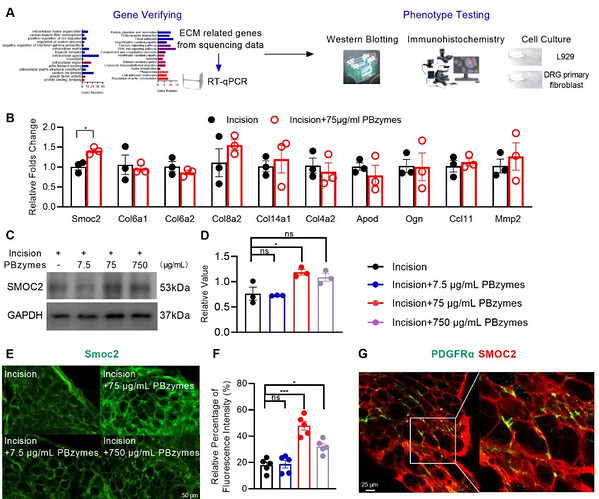
基于转录组富集结果,研究者围绕 ECM 关键分子 SMOC2 开展多维度分子验证(图 6A)。RT‑qPCR 结果显示,PBzymes 显著上调 DRG 中 Smoc2 的 mRNA 水平(图 6B)。Western blot 证实,仅 75 μg/mL 有效镇痛剂量可显著提高 SMOC2 蛋白表达,与行为学剂量效应一致(图 6C–D)。免疫荧光染色及定量显示,PBzymes 处理后 DRG 内 SMOC2 荧光强度明显升高(图 6E–F)。共定位实验显示,SMOC2 与成纤维细胞标志物 PDGFRα 共定位,证实其主要来源于 DRG 成纤维细胞(图 6G)。同时,初步安全性评价显示 PBzymes 不影响小鼠体重与主要脏器形态,具备良好生物相容性。该部分结果明确PBzymes 可特异性上调 DRG 成纤维细胞 SMOC2 表达,且表达变化与镇痛效应、剂量依赖性完全匹配。
06 PBzymes 促进成纤维细胞分泌 SMOC2
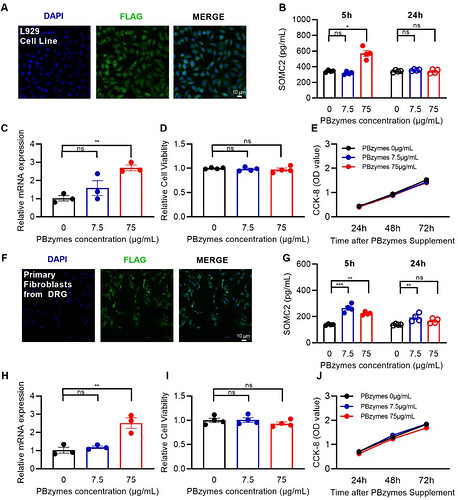
考虑到 SMOC2 为分泌型蛋白,研究进一步在 L929 成纤维细胞系与原代 DRG 成纤维细胞中验证 PBzymes 对 SMOC2 分泌的调控作用(图 7A, F)。结果显示,PBzymes 处理可显著提高两类细胞的 SMOC2 分泌水平,并上调 Smoc2 mRNA 表达,提示 PBzymes 可直接促进 SMOC2 合成与分泌(图 7B–C, G–H)。CCK‑8 检测证实,75 μg/mL PBzymes 不影响细胞活力与增殖,无明显细胞毒性(图 7D–E, I–J)。上述结果表明,PBzymes 可直接、安全地调控成纤维细胞分泌 SMOC2。
07 DRG 特异性敲低 Smoc2 逆转 PBzymes 的镇痛效应
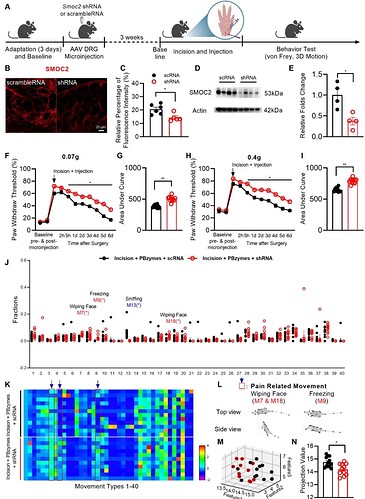
为验证 SMOC2 是 PBzymes 镇痛的必需靶点,研究采用 AAV 介导 shRNA 在 DRG 特异性敲低 Smoc2(图 8A)。免疫荧光与 Western blot 证实 SMOC2 表达被显著下调,敲低效率可靠(图 8B–E)。行为学结果显示,SMOC2 敲低可完全逆转 PBzymes 对机械性痛觉超敏的缓解作用,缩足频率恢复至切口组水平,证实镇痛效应依赖 SMOC2(图 8F–I)。3D 运动捕捉分析显示,SMOC2 敲低后疼痛相关行为占比显著回升,运动模式重新呈现疼痛异常特征(图 8J–N)。结合外源性 SMOC2 可复刻镇痛效应的补充实验,该部分结果证明 SMOC2 是 PBzymes 发挥镇痛作用的必要且充分靶点。
08 研究结论与意义
|研究结论|
1.首次证实普鲁士蓝纳米酶(PBzymes)可显著、持续、选择性缓解术后机械性痛觉超敏,且镇痛作用呈现钟形剂量效应,不影响热痛觉传导。
2.阐明 PBzymes 可经坐骨神经转运并靶向富集于背根神经节(DRG),通过上调 DRG 成纤维细胞中 SMOC2 的表达与分泌发挥镇痛效应。
3.证实 SMOC2 是 PBzymes 发挥镇痛作用的必要且充分靶点,其敲低可完全消除镇痛效果,外源性补充 SMOC2 可精准复刻镇痛表型。
4.揭示 PBzymes 可通过抑制 DRG 感觉神经元异常兴奋,改善术后自发性疼痛及伴随的焦虑样行为,实现多维疼痛行为调控。
5.验证 PBzymes 生物安全性良好,对细胞与主要脏器无明显毒性,具备临床转化潜力。
|研究意义|
1. 提出全新镇痛策略: 首创“内源性镇痛”非阿片类方案,不依赖外源性镇痛药物,通过激活机体自身镇痛通路实现长效镇痛。
2. 揭示全新分子机制: 首次建立 “PBzymes–DRG 成纤维细胞–SMOC2–神经元兴奋性” 的完整镇痛信号轴。
3.拓展纳米酶应用场景: 首次将普鲁士蓝纳米酶用于术后疼痛调控,拓宽纳米酶在外周神经调控与围术期医学 中的应用边界。
4.提供临床转化价值: 基于 FDA 批准的普鲁士蓝改造而来,安全性明确、靶向性强、无成瘾风险,为解决阿片类药物副作用 提供替代方向。
5.方法学创新: 结合 3D 运动捕捉 AI 行为学分析,实现术后疼痛客观化、精细化、无偏量化评估 ,为疼痛研究提供新工具。
09 Bayone 助力科研
该研究论文应用了一湾生命科技(BAYONE)自主研发的 3D-AI 小鼠行为分析系统,为术后疼痛行为表型的精细化研究提供了重要工具支撑。一湾生命科技致力于通过 AI 技术,为脑科学及脑疾病研究等领域提供新一代更高效、更精准的仪器、软件、服务和标准。一湾生命科技专注于推动 AI 精细行为学技术在神经疾病模型的研究中发现新的生物标志物、表型鉴定及愈后评估等方面的应用。如果您对这一技术感兴趣,或者需要进一步了解 “如何通过专业行为学软件,复现类似研究中的术后疼痛行为检测范式”,或针对特定行为学实验定制分析方案,欢迎了解更多关于 BehaviorAtlas 3D-AI 动物行为分析系统 的信息!
BehaviorAtlas 3D-AI 动物行为分析系统是国内首家 3D-AI 精细行为学分析系统,可以在三维层面分析动物的精细行为;追踪 16+ 个身体点,实现行为全面量化;提取 40+ 种行为亚型,包括嗅探、梳理、跳跃等行为;计算 100+ 种参数,捕捉动物行为的每一个细节;输出专业级可视化图表,满足SCI论文发表要求。 目前,BehaviorAtlas 3D-AI 动物行为分析系统已经在大、小鼠、非人灵长类动物、犬类等模式动物上,针对自闭症、帕金森症、抑郁症、老年痴呆、脑出血等疾病模型以及精神类药物筛选上进行了多种应用。在此,我们也感谢 BehaviorAtlas 的用户对我们系统的关注和支持,希望 BehaviorAtlas 能够帮助更多的科研人员去解答生命科学中的难题。如果您希望深入了解其在动物行为研究中的应用,我们非常欢迎您进一步探索!
为了帮助您获取更多信息,我们提供了便捷的联系方式。您可以通过公众号私信与我们交流,或者直接扫描下方的微信二维码,我们的专业团队将竭诚为您提供更多信息和帮助。
参考文献:
————————————————
Gu X, Du Z, Liu Y, Han X, Chaudhury D, Wang F, Li Q, Yan H, Cai X, Yu W, Zhang S. Prussian blue nanozymes alleviate postoperative pain via upregulating endogenous SMOC2 secretion in dorsal root ganglion fibroblasts. J Adv Res. 2026 Feb 18:S2090-1232(26)00177-3. doi: 10.1016/j.jare.2026.02.045. Epub ahead of print. PMID: 41720157.