Biological Psychiatry 综述:侵入性计算精神病学
摘要
计算精神病学是一个相对较新但又多产的领域,旨在用关于大脑的正式理论来理解精神疾病,在过去的十年中看到了巨大的增长。尽管一开始很兴奋,但计算精神病学取得的实际进展似乎停滞不前。与此同时,对人脑的了解也得益于颅内神经科学的最新进展。具体来说,侵入性技术,如立体定向脑电图、皮质电图和深部脑刺激,提供了一个独特的机会来精确测量和因果调节的人类大脑中的神经生理活动。在这篇综述中,我们总结了计算精神病学和侵入性电生理学的进展和缺点,并提出它们的结合提出了一个非常有前途的新方向——侵入性计算精神病学。这种方法的价值至少有两方面。首先,它通过提供对神经活动的时空精确描述,推进了我们对心理状态的神经计算的机制理解,这是传统上使用非侵入性技术无法实现的。其次,它提供了一种直接和间接的方法,通过刺激算法定义的神经区域和回路(即算法靶向)来调节大脑状态,从而提供因果和治疗的见解。然后,我们将抑郁症作为一个用例,其中计算和侵入性方法的结合已经显示出了最初的成功。最后,我们概述了这一令人兴奋的新领域的未来发展方向和路线图,并对诸如伦理问题和研究发现的普遍性等问题提出了警告。
1. 计算精神病学:十年过去了,现在呢?
认识到计算方法和理论可以对我们理解大脑和相关疾病做出有意义的贡献,这已经改变了精神病学的游戏规则。计算精神病学是由计算神经科学和精神病学结合而来的一个新的研究领域,旨在用最先进的计算模型和理论来改变精神病学研究。事实上,已经取得了大量令人印象深刻的进展,从使用机器学习(ML)的生物标志物研究到发现更丰富和更深入的内表型的机制研究。在文化上,计算科学家和临床医生之间日益增加的对话已被证明是互利的,这使得基础研究更加与临床相关,而临床研究更加严格和机械性。在接下来的章节中,我们将讨论计算精神病学需要什么,以及它可能如何向前发展,并考虑到某些障碍。
1.1 精神病学中的计算模型:一本入门书
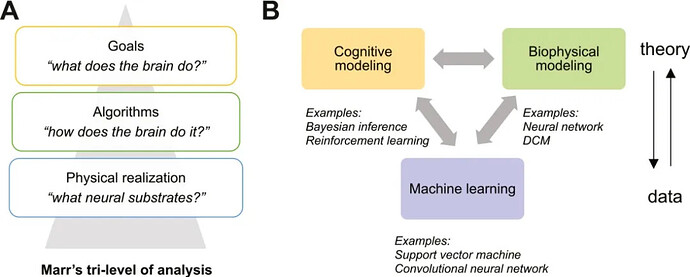
计算精神病学在很大程度上依赖于Marr的三重分析框架(图1A),该框架提出,要研究任何智能系统(例如,人类大脑),必须考虑多个层次的解释,包括系统的目标(“为什么”),算法层次(“如何”),最后,物理实现(例如,神经基质,“在哪里”)。这一想法在神经科学中得到了广泛的影响,因为它为绘制计算、行为和它们的神经基质之间的关系提供了一个明确的蓝图。基于这个框架,今天的计算精神病学涵盖了3个主要的研究领域(图1B):认知模型解释行为(例如,强化学习[RL],贝叶斯推理、漂移扩散模型),直接解释神经活动的生物物理模型(例如,动态因果模型[DCM],神经网络),和使用ML进行数据挖掘的统计模型(例如,预测生物标志物研究)。
认知和生物物理模型都被认为是自上向下的,因为它们通常需要明确的基于理论的假设检验;它们还需要在精心设计的实验范式(例如,决策任务)下收集神经行为数据。RL是计算精神病学研究中最流行的认知和行为建模方法之一。这些模型通常旨在通过寻找一个基于学习而更新的价值信号来解释人们的选择行为(例如,使用预测错误)。相比之下,生物物理模型通常关注于直接解释神经活动。作为这样一个例子,DCM使用生成模型来对神经元种群之间的有效连通性或方向性进行统计推断。在认知模型和生物物理模型中,人们通常可以比较各种各样的模型的设置(即模型比较),它们代表了关于正在研究的认知或神经过程的不同假设。
(A)有影响力的Marr的三重分析为计算精神病学奠定了理论基础,它提出,要研究大脑,人们必须考虑多个层次的解释,包括目标(“为什么”),算法表示(“如何”),最后是物理实现(例如,神经基质,“在哪里”)。(B)认知模型,如贝叶斯和强化学习,生物物理模型,如动态因果模型(DCM),以及机器学习模型,如支持向量机或深度学习,构成了神经精神病学研究中常用的3个主要模型类别。
ML通常被认为是数据驱动的和自下而上的,可以包括在实验室环境中通常收集的数据类型(例如,电子病历)。ML技术主要有两个类:无监督学习和监督学习。无监督学习通常用于识别未标记数据中的隐藏结构。一个例子是聚类分析(例如,k-means),它将数据标记为同一组中的个体彼此最相似,与其他组中的个体最不相似。在计算精神病学研究中,无监督的方法已被用于发现患者中的新亚型。在有监督的学习中,算法需要一个训练数据集来学习如何对不可见的数据进行预测(因此是有监督的)。例如,通过在现有数据集(训练数据)中找到对选择性5-羟色胺再摄取抑制剂有反应者和无反应者的分类模式,我们可以预测一个数据未被模型看到的新患者是否会对选择性5-羟色胺再摄取抑制剂有反应。有许多算法可供选择,如支持向量机和神经网络(包括卷积神经网络)。
1.2 障碍
尽管取得了这些进展,计算精神病学的几个方面仍然停滞不前。首先,迄今为止,大多数基于ML的研究还不能提供可解释性或机制性的解释。其次,理论驱动的计算精神病学研究大多采用了一种与心理健康相关的特定类型的模型和范式,即那些围绕RL和基于奖励的任务的模型。尽管它们最初取得了成功[例如,解释快感缺乏症],但它们提供了一个单一主题的观点,不能解释精神障碍中主观状态的复杂性,即各种强调错误信念的重要性和不确定性在调节精神病理学中的作用。第三,大多数人类研究仍在使用功能磁共振成像(fMRI)或其他非侵入性神经技术(如脑电图[EEG])时间或空间分辨率,并在很大程度上保持相关性。因此,对于神经精神疾病中潜在的神经激活的详细描述和计算参数(如预测错误)的真实因果关系的证明仍然缺乏。最后,采用计算范式、模型或理论的治疗研究(即临床试验)仍然稀缺,这限制了我们将研究结果转化为精神卫生保健的能力。
1.3 展望未来
鉴于上述现状,计算精神病学的迫切需要是提供神经精神疾病的机制见解,也可以直接告知因果索赔和治疗策略。人类颅内研究提供了一种独特和互补的方法,可以在更精细的时间和空间分辨率(例如,单个神经元峰值),因果操纵(例如,作为扰动,刺激),以及重要的治疗潜力(例如,刺激作为治疗)。在这篇文章中,我们的目标是提供一个路线图,说明这两个领域如何成为侵入性计算精神病学(ICP)的一个新领域,为这两个领域产生切实的改进,最终有利于精神病学治疗策略。
2. 人类颅内神经科学:不寻常的嫌疑人
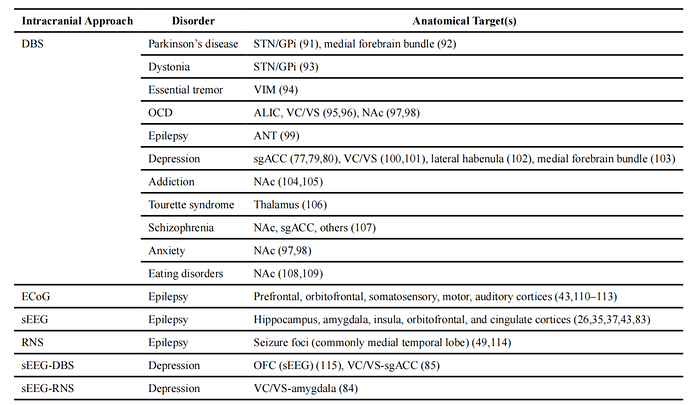
最近神经科学研究的一个特别富有成果的路线来自于人类颅内研究,它利用了功能性神经外科干预。在这些过程中,患者被植入具有高解剖精度的电极,以允许电生理监测和/或靶向对受损脑区域的电刺激。这些记录与功能磁共振成像等无创神经成像技术相比,具有主要优势。具体来说,颅内信号提供了神经元活动的直接读出,具有优越的空间(毫米)和时间(亚毫秒)分辨率和更高的信噪比,并且更容易在生物学上解释。在这里,我们讨论了最常用的颅内方法(深部脑刺激DBS和颅内脑电图iEEG)(术语表见表1,每种方法的解剖目标和患者群体见表2)。也存在其他侵入性干预措施,但他们的在人类神经科学中的应用仍在很大程度上未被探索,并且超出了本综述的范围。
本表概述了目前用于治疗神经和精神疾病的颅内干预措施,包括最常见的解剖靶点。
2.1 人类颅内干预措施的类型
DBS主要用于治疗运动疾病(帕金森病[PD])、肌张力障碍、特发性震颤)的症状,尽管人们对其在强迫症(OCD)和治疗难治性抑郁症中的应用越来越感兴趣。DBS干预通常针对皮层下结构,如丘脑下核和邻近区域,但也可用于针对深层皮层结构,如胼胝体下扣带皮层。DBS提供了对大脑区域的途径,这些区域对于行为的许多方面都很重要,因此提供了一个非常有价值的研究机会。局部场电位(LFPs)、单单位神经元峰值和神经化学信号都可以用DBS平台记录下来。
皮质电图(ECoG)和立体定向EE图(sEEG)主要在顽固性癫痫患者中进行,对电生理活动的有创监测有助于确定局灶性癫痫发作的来源。与DBS相比,iEEG具有几个独特的优势。首先,患者监测通常持续几天或几周,这为研究提供了一个相当宽的时间窗口。其次,iEEG比DBS提供了更广泛的解剖覆盖范围,如眶额叶、颞叶和扣带-岛叶皮质(表2)。典型的植入可以包括跨越多个区域的几十到几百个电极,允许研究全电路的活动。
2.2 神经生理学信号的类型
使用侵入性的方法可以记录几种不同类型的神经活动。DBS手术可能允许进行LFP、单单元和快速扫描循环伏安法(FSCV)记录,而iEEG手术目前允许进行LFP和单个单元记录。
LFPs,反映了电极附近数十万个神经元的协调激活,提供了一个大脑活动的中尺度测量。lfp可以揭示认知过程中神经活动的振荡成分(例如,啮齿动物、猴子和人类的空间导航和探索中的[4-8Hz]振荡]。此外,sEEG记录的分布式特性为检查整个电路范围内的活动和跨区域的功能通信(例如,振荡相干性)打开了大门。对LFP活动的频率成分的检查可以为了解神经元激活的不同方面对计算的贡献提供更多的见解。考虑到LFPs和fMRI血氧水平依赖性(BOLD)信号之间的复杂关系,这一点尤其相关,后者是计算精神病学中最常用的神经测量方法。一些研究表明,LFPs的高频活动(或高伽马,通常是70-200Hz)成分是皮层激活的关键标志,反映了单单位峰值和BOLD活动。其他的研究也将这种关系扩展到高频活动之外,并显示了BOLD信号与伽马(30-70Hz)和较低频率的功率之间的关联,较低频率的激活主要反映了BOLD的增加。最后,这种关系可能在不同的皮质区域而有所不同。综上所述,这些结果强调了分布式LFP记录可以很好地揭示更详细和复杂的神经元活动描述,并强调了对神经元激活的精确解剖定位的必要性。
在癫痫手术中,使用专门的研究电极(即LFP)电极与多电极探针(即Behnke-Fried电极)或以研究为重点的植入。这些方法为单个神经元的编码特性提供了独特的途径,揭示了神经元在记忆、抽象、空间导航和其他认知过程中的作用,并在脑机接口应用中得到了更广泛的研究。
最后,在DBS手术中使用特殊碳纤维电极的新型电化学方法允许对神经化学信号进行亚秒估计,这些信号对认知和行为的几个方面至关重要,即多巴胺和血清素。
2.3 现有的人类侵入性计算神经科学研究
最初的努力是将颅内记录与人类行为的计算模型相结合。脑电图研究揭示了使用RL模型和侵入性LFP记录的纠正和惩罚相关计算的神经生理学基础。研究也已经开始使用FSCV方法来研究神经化学信号,如多巴胺、血清素和奖赏计算之间的关系。这些研究表明了将计算行为描述与颅内方法相结合的可行性,并为本文提出的计算精神病学方法奠定了重要的基础。
3. ICP的机理值
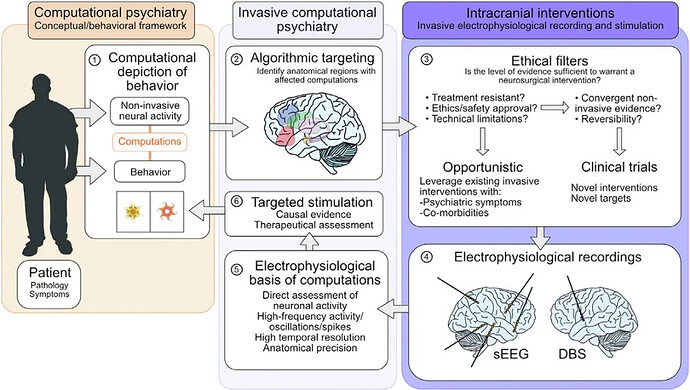
由在本节中,我们将讨论与ICP相关的机遇和挑战,这是神经精神病学研究中计算建模和颅内记录的新组合(图2和表3)。
计算精神病学提供了定量模型,描述行为并指定潜在的计算(1),并允许识别受疾病状态影响的区域和计算(2)。与现有的颅内入路(3和4)的结合,为更详细地描述行为的神经生理学基础(即跨频带的活动、精细的时间分辨率)及其相关计算(5),以及解剖靶向神经刺激范式的发展(6)打开了大门(6)。目前,这种方法可以通过利用接受神经外科干预的患者中存在的精神共病,或者如果有足够的证据支持新的侵入性临床试验,则通过开发临时干预来进行。DBS,脑深部刺激;sEEG,立体定向脑电图。
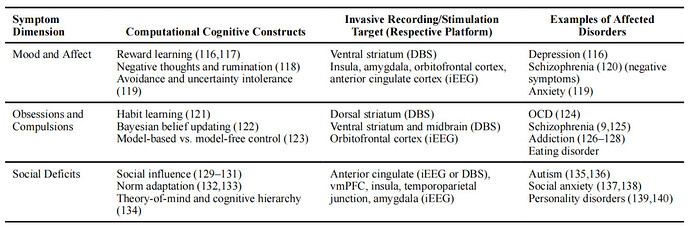
因为大多数精神症状都是经诊断的,在这里,我们列出了特定症状维度、计算定义的结构和相关的大脑区域/回路之间的初步映射,这些区域可以通过人类颅内记录或刺激来定位。随着计算精神病学和人类颅内研究的发展,我们对这些映射的知识将继续发生变化。DBS,脑深部刺激;vmPFC,腹内侧前额叶皮层。
3.1 对计算精神病学的好处
迄今为止,计算精神病学的研究主要依赖于基于模型的脑成像分析(例如,功能磁共振成像)和行为数据。尽管与生物精神病学研究中对这些数据类型的传统无模型分析相比,这是一个重大进步,但仅用计算建模并不一定提供一种方法来检验因果关系或大幅提高成像数据的可解释性。因此,计算精神病学可以从多个方面受益于侵入性神经科学。
首先,增加的生物细节获得的时空分辨率的颅内记录将允许推理超出功能定位(例如,腹内侧前额叶皮层受损障碍X)通过提供一个更细致的视图的神经计算潜在的行为(例如,高频活动值计算腹内侧前额叶皮层受损障碍X)。高信噪比和时空分辨率也使神经数据更适合于生物物理建模,这是计算精神病学研究中常用的另一类重要模型。来自iEEG的多区域记录对于这一目的尤其重要,因为许多这些生物物理模型旨在理解大脑中的局部和全局电路级机制。例如,目前,DCM主要应用于fMRI或头皮脑电图数据。相比之下,颅内记录的神经信号为DCM的单个神经元和种群水平的活动提供了更好的代理,这是基于对神经元种群的假设而建立的。由于类似的原因,其他类型的生物物理模型也可以受益于颅内信号。
接下来,能够直接剧烈地扰乱人类大脑中的神经元活动,为计算精神病学提供了一个独特的机会,以精确地提出关于神经计算机制的因果主张。我们可以想到的一个直接的例子是,在确定了计算参数(例如,预测错误)和神经记录之间的关联后,我们现在可以对目标神经元应用瞬时(通常是亚临床阈值)刺激,并检查该任务参数的编码现在是否受到干扰。如果后行为(例如,奖励学习)发生改变,从而模仿人们在特定患者群体中看到的情况,那么这个结果可以提供因果证据,证明在该患者群体中观察到的行为障碍可能是由于目标脑区神经元的扰动造成的。
最后,随着慢性刺激已经成为一种越来越流行的治疗方式,ICP可以直接在相关的行为背景下解决与治疗相关的问题,特别是对于那些被认为有治疗困难的患者(这个概念称为算法靶向)。例如,治疗强迫症患者现在可以受益于长期植入DBS设备提供刺激神经电路的行为控制,同时执行神经计算通知任务,如那些旨在探测毅力可以证明DBS是否确实有效地减少核心强迫症症状和强迫症等行为。此外,一些设备(例如,美敦力知西普PC神经刺激器[美敦力公司],神经节奏反应性神经刺激[RNS系统;神经节奏])也允许慢性记录,这为自然环境中的纵向调查打开了大门。综上所述,颅内神经科学可以有效地支持计算精神病学在时间和空间精度、因果推理和治疗机制方面提出的机制主张。
3.2 对颅内神经生理学的好处
目前,颅内干预通常是针对单一或少量的基于功能定位理念(即每个心理功能特定位于大脑的特定部位)的解剖目标(如PD的丘脑底核)。这一原理为早期的认知神经科学奠定了基础;然而,它已经开始显示出其局限性,因为通常,相同的大脑区域(或回路)似乎能够实现许多不同的功能。基于文献回顾到目前为止,我们建议应用计算框架可以有利于颅内神经科学通过允许更深层次的理解颅内神经活动机械与算法编码行为或疾病症状(例如,奖励功能障碍和快感缺乏),一种方法已经被证明是富有成效的非侵入性研究。
因此,计算精神病学方法可以有可能揭示干预的新算法目标(图2和表3)。这特别指的是在一个由特定算法实现的精神状态的背景下,针对大脑区域或其连接的目标。表3提供了一些例子,包括RL、奖励处理和快感缺乏之间的关系,以及偏不确定性计算、威胁回避和焦虑之间的关系(值得注意的是,我们在这里关注快感缺乏或焦虑等症状,考虑到障碍的异质性,这可能是经诊断的)。在这里,算法靶向策略将通过评估适当的行为背景下(如基于RL的奖励计算)的大脑活动来揭示刺激目标(如中边缘区域,如腹侧纹状体),这对于连接神经生物学和行为/症状水平的刺激效应至关重要。类似的症状激发的思想长期以来一直被用于精神病学,尽管没有考虑算法或计算机制。很有可能这样就可以确定新的刺激策略。例如,即使持续高频刺激是DBS的主要策略,其他刺激策略(例如,theta突发刺激提供颅外)可能不同有效的治疗精神疾病的参与神经振荡的认知过程在精神疾病的改变。
算法目标的概念并不限制在解剖上限制或功能上分离的大脑区域。相反,它还允许针对区域之间的功能连接或整合。这源于所有算法都需要消息传递,而消息传递则意味着连通性。由此可见,算法的目标可能是支持大脑中分布式处理的连接。精神疾病中的连接障碍可以从韦尼克分离假说精神下的白质束中断和白质营养不良,到一系列突触病变(如精神分裂症、帕金森病)所暗示的功能解体或连接障碍。在这种情况下,多区域、多电极平台(如sEEG)变得至关重要,因为机会将通过电路和网络级的记录和刺激而出现。这与目前的精神病学DBS方法形成了对比,后者几乎完全是单一的目标(表2)。方便,精神并发症如抑郁症非常高患者接受sEGG,终生患病率30%到35%的人口研究癫痫患者,甚至更高的利率(w50%-55%)的患者在三级中心。这提供了一个很好的机会来检查算法目标使用全电路记录来解决精神相关的问题。
4. 转化和临床效用
如上所述,所提出的ICP方法的主要优势在于基于模型的任务状态下的全电路大脑活动描述,具有详细的神经生理学描述以及刺激能力,提供了因果和治疗的见解。虽然我们不能详细回顾所有的临床应用,但表3提供了神经计算、症状和一些DBS或iEEG靶向的疾病例子之间的初步映射。我们使用抑郁症——一种已经使用计算和侵入性方法进行研究的疾病——来展示两者结合的优势。
4.1 案例研究:抑郁症
重度抑郁症是一种复杂的疾病,以一系列症状为特征,包括抑郁情绪低落、快感缺乏、反刍和能量下降。抑郁症的计算特征已经成功地将这些临床症状量化为异常的基于奖赏的计算,如改变的奖励预测和反事实错误、基于模型的推理、学习过程中的先前更新和获得性无助。这些都伴随着神经活动的潜在改变,如纹状体中fMRI-BOLD活动的差异,以及奖赏引导行为中脑电图波形的改变。此外,最近扩展的RL模型关注选择行为——比如那些关注情绪或主动推理模型的信念和选择——可能提供一个有价值的方法来量化和确定这些异常计算和主观状态之间的联系。这些情绪和抑郁的计算特征为揭示抑郁症的深层表型和生物标志物铺平了道路,有助于优化药物治疗,并对该疾病的病因提供了更深层次的机制理解。抑郁症临床症状的其他方面,如身体或躯体症状和社会缺陷,也是该疾病的核心,但计算模型仍然在很大程度上研究不足。
在侵入性方面,在过去的几十年里,人们已经多次尝试开发治疗抑郁症的神经刺激疗法。针对胼胝体下扣带皮层为目标的DBS治疗,基于与负面情绪相关的下胼胝体下扣带皮层激活的影像学发现。尽管这种方法的有效性各不相同,但干预在一些患者中非常成功,这表明需要更好地评估不同亚型的疾病表现,并进行更个性化的治疗。此外,正在进行的临床工作仍然集中于基于单区域的解剖靶向,这可能很快会被电路水平的个性化定位所取代(例如,识别和靶向异常计算的接触)。补充方法使用收敛建模和刺激方法,利用癫痫sEEG干预来开发治疗抑郁症的个性化刺激方法。
未来的抑郁症研究可以从几个方面受益于ICP。首先,更多的研究可以同时部署基于计算信息的任务来评估情绪和侵入性记录。与传统的行为或成像方法相比,这种方法将揭示抑郁情绪和快感缺乏的神经机制的粒度。第二,抑郁症的刺激研究可以受益于算法靶向的想法,并使用计算驱动的任务来增强刺激效果。事实上,类似的概念已经被应用于恐惧记忆的研究,即在条件刺激下刺激时,消失会增强。虽然不是计算性的,但这项工作证明了将刺激置于相关的行为环境中的可行性(例如,在消极情绪或奖励学习中特别应用DBS),以产生更好的治疗效果的可行性。最后,该联合方法提供了公开的行为指标(如情绪)和神经活动之间的中间机制联系,这可能有助于建立神经功能障碍的模型,识别潜在的计算生物标志物,并有助于概括对个别患者的见解。
5. 限制和未来的发展方向
正如在本综述中所强调的那样,迫切需要在精神病学中对计算和侵入性方法进行更系统和全面的整合。我们也认识到与ICP相关的局限性。首先,大多数参与者在ICP研究仍仅限于个人癫痫或运动障碍患者通常有神经缺陷在基线(例如,改变时间和海马活动在癫痫和多巴胺水平降低PD),减少能量水平和增加认知困难完成任务,和有限的时间参与研究(例如,通常不到20-30分钟的术中记录)。然而,人们可以通过仔细考虑实验细节(例如,通过设计稳健而快速和可访问的任务,并包括适当的控制条件)来克服这些挑战。
另一个潜在的障碍是可以获得清醒的DBS手术或4级癫痫中心(即,由全国癫痫中心协会认证的癫痫护理水平最高的中心)。对于某些方法,如FSCV方法或多电极植入法的电化学记录,这需要高度专业化的研究和临床专业知识。然而,这些挑战可以通过在计算团队和临床团队之间建立强大的合作来克服,首先是在具有临床和研究组成部分的机构内,然后随着这个新领域的发展逐步跨机构进行。
考虑到在患者中进行研究的必要性,以及必须与参与研究的患者建立双重临床-研究关系,在ICP中,伦理考虑尤为重要。特定领域的指南已经开始发展,最近审查建立原则颅内研究,如需要建立明确区分临床和研究工作(和人员角色,医生的调查人员),需要隔离临床决策从研究目标(除了研究动机的颅内研究),和健壮的和标准化的同意程序。对于这里提出的脱靶算法靶向方法,特别重要的是需要监测刺激的潜在副作用。
展望未来,我们希望ICP将在未来几年看到快速增长。ML现在是一种成熟的方法,可以常规地用于预测患者大脑中的个体“热点”,从而最有效地刺激以达到治疗效果。这一想法的一个更先进的应用是设计闭环系统,自动计算神经和行为指标,并随时优化对个体患者的刺激,这是神经调节治疗的“圣杯”。在理论驱动的建模领域,ICP将揭示在神经元和亚秒水平上关于服务于不同认知功能的神经计算的更精细的细节。最后,需要进行包括神经调节和计算表型在内的临床试验,以验证算法靶向的想法,这将有望进一步提高个体化、封闭的循环系统的有效性。
参考文献:Saez I, Gu X. Invasive Computational Psychiatry. Biol Psychiatry. 2023 Apr 15;93(8):661-670. doi: 10.1016/j.biopsych.2022.09.032. Epub 2022 Oct 8. PMID: 36641365; PMCID: PMC10038930.