Nature Reviews Neuroscience(IF:34.7) | 为什么女性生完孩子后会「母爱泛滥」?
摘要:我们正在目睹与怀孕和生育有关的神经生物学过程的科学兴趣急剧增加。越来越多的证据表明,在分娩前后,初为人母的母亲会经历一种与母性行为相关的特定神经解剖学变化模式。在这里,我们提供了母性的人类神经生物学适应的概述,重点是怀孕相关的类固醇和肽激素之间的相互作用,以及大脑中的神经可塑性。我们讨论了哪些大脑可塑性机制可能是MRI检测到的结构变化的基础,哪些激素系统可能导致这种神经解剖学变化,以及这些大脑机制如何与母性行为联系起来。本综述提供了一个总体框架,可作为未来调查的路线图。
01 引言
成为母亲在生理和心理层面上都是一个转折性的事件。新生儿的到来需要母亲进行一系列行为适应,以确保后代的福祉。在过去十年中。核磁共振研究一致表明,女性的大脑在怀孕和产后也经历了实质性的神经解剖学变化。这些大脑结构变化和行为适应伴随着激素的极端波动,而激素是大脑可塑性的有效调节剂。然而,激素、大脑可塑性和向母亲转变过程中的行为之间的具体关系仍然需要解开大脑可塑性是指神经系统通过调节细胞功能、大脑结构和连通性来适应生理和环境需求的终身能力。100多年来,激素一直被认为在早期和青春期等敏感发育时期协调神经可塑性。怀孕期间的荷尔蒙波动超过了人类一生中任何其他神经内分泌事件。然而,研究人员直到最近才开始考虑怀孕和产后时期也是激素驱动的大脑可塑性的敏感窗口的可能性。非人类动物模型为理解激素对大脑和母亲行为的影响铺平了道路。对啮齿动物的研究表明,怀孕激素启动了一个被称为“母性照顾回路”的神经回路,它促进了母性行为的发生。母性照料回路的功能激活伴随着结构神经可塑性,包括脑细胞增殖和形态的改变。在目前的工作中,我们提出了细胞水平上激素驱动的神经可塑性可能转化为人类神经解剖学和行为变化的潜在途径。我们首先回顾了与人类怀孕和产后有关的神经解剖学和激素变化的最新证据。必要时,会讨论功能性MRI脑改变,但这超出了本综述的范围。接下来,我们概述了妊娠相关激素促进负责母性行为的神经回路激活的途径。然后,我们描述了这些激素如何触发神经可塑性机制,转化为啮齿动物母体大脑中的神经元和胶质结构变化。最后,我们讨论了激素、神经可塑性和人类母性行为之间的潜在联系,并提出了一系列问题,可以作为未来研究的路线图。
02 母亲的神经解剖学变化
几十年来,成为母亲这一改变人生的事件一直不在磁共振研究的范围之内。第一个描述与怀孕有关的广泛而明显的神经解剖学变化的对照神经成像研究仅在几年前发表。”我们首先总结了第一项研究的主要发现,以及随后的努力,以了解人类怀孕和产后期间大脑发生了什么。怀孕会导致母亲大脑结构的变化。与未分娩的妇女相比,首次分娩的母亲在怀孕前和分娩后2-3个月的评估中显示出广泛的灰质脑容量减少。与怀孕相关的大脑减少是显著的,总皮质灰质体积平均减少3%”。这种灰质体积减少主要位于中线区域(从内侧前额叶皮层(mPFC)延伸到前扣带皮层,从楔前叶皮层延伸到后扣带皮层)、外侧前额叶皮层(主要是额叶中下回)、上颞叶皮层和中颞叶皮层(延伸到脑岛,梭状回和颞顶叶交界处)。灰质减少也会影响皮层下区域,如海马体(和海马旁回)、腹侧纹状体(包含伏隔核的皮层下区域)和背侧纹状体,特别是尾状核。
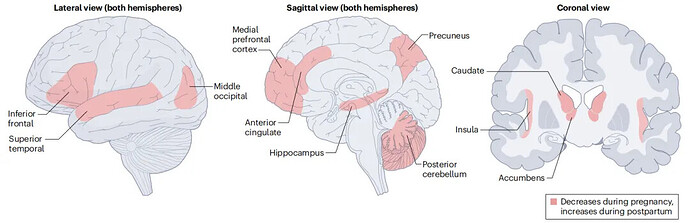
形态计量学研究还显示,这些灰质减少与皮层变平同时发生,类似于青春期发生的情况,也就是说,大脑皮层变薄、不那么弯曲,脑沟变短、变窄、变浅。这种明显的皮质变平是持久的,在分娩后仍会持续数年纵向研究比较了分娩后和几个月后女性的大脑解剖结构,结果显示,在整个产后期间,大脑容量会增加。具体来说,虽然母亲在产后立即与非母亲相比显示出灰质体积减少,但随着产后时期的进展,这种体积差异部分减少。许多在怀孕期间灰质体积减少的区域与产后增加的区域重合(图1)。这些区域包括楔前叶、颞上回、额下回和内侧前额回,延伸到前扣带、内侧颞区(包括海马、海马旁回和岛)、视觉区域,如枕中回、小脑后部、腹侧纹状体(包括伏隔核)和背侧纹状体(包括尾状核)。这些发现绘制了一个动态轨迹,在怀孕期间体积减少,至少部分,倾向于在产后恢复(图2)。重要的是,灰质在人类怀孕和产后期间变化的完整纵向时间过程仍有待阐明。
阴影区域表示脑灰质体积为据报道,在怀孕期间会减少,在产后会增加。值得注意的是,该图只显示了同时的减少和增加已经被记录下来,不包括其他在怀孕期间减少但在产后没有增加的大脑区域,反之亦然。
03 神经解剖学和母性行为
在向母性过渡期间,灰质的变化可能会促进母性行为。在人类中,与怀孕相关的神经解剖学变化程度与不同的自我报告的母婴关系的间接测量有关,包括更高的依恋质量,对新生儿的敌意更低,以及增加的社会选择性(例如,对亲密朋友或家人的强烈偏好)。在产后期间,由下丘脑、杏仁核和苍白球组成的中脑群的灰质体积增加,与母亲将更多的积极添加剂归因于婴儿有关。”此外,女性在怀孕期间伏隔核的体积减少与婴儿出生后对婴儿照片的反应增加的神经激活呈正相关。总而言之,在怀孕期间和产后观察到的大脑结构变化可以作为一种神经调节,促进对新生儿的敏感和及时的行为。
04 神经解剖学和妊娠激素
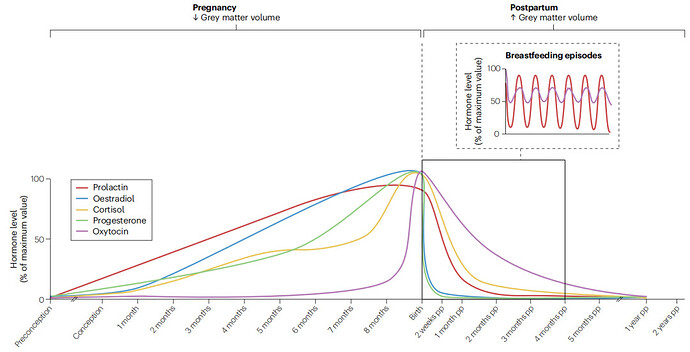
人类怀孕是一个动态而协调的过程,涉及巨大而复杂的激素波动。然而,当采用全景视图时,我们看到分娩前后激素波动的明显变化(图2)。在怀孕期间上调的类固醇激素在产后急剧下降。同样,催产素和催乳素的水平也有上升和下降,但它们在产后的分泌与母乳喂养和母婴互动有关。值得注意的是,图2所示的激素时间线代表了外周循环中发生的波动。在类固醇激素的情况下,这些变化可能类似于脑内发生的波动,因为类固醇很容易通过不饱和过程穿过血脑屏障。相反,蛋白质激素主要在大脑中产生,然后输出到外周。在这种情况下,通常假设外围水平在某种程度上表示中央生产。然而,我们仍然不知道外围和中枢水平之间的确切关系,外推应谨慎。
母亲的大脑结构变化通常归因于怀孕激素。一些啮齿类动物的研究已经记录了激素——包括雌二醇、黄体酮、皮质酮、催乳素和催产素——如何在向母性过渡的过程中触发神经可塑性。然而,在人类神经影像学研究中,内分泌因素几乎从未被考虑过,即使被收集起来,也很少被考虑。尽管如此,一些新出现的证据表明,怀孕激素与人类大脑结构变化之间存在关系。例如,在妊娠晚期,与妊娠相关的灰质总体积减少与较高的循环雌二醇水平有关。”此外,从怀孕期间灰质体积减少到产后灰质体积增加的转变与分娩前后激素环境的明显变化是一致的(图2)。最后,怀孕期间和青春期(另一个类固醇激素波动最大的时期)大脑结构变化的相似性表明,重叠的激素因素可能会促进这两个时期观察到的神经变化。总的来说,这些观察结果表明,激素因素可能会引发人类怀孕期间的神经可塑性。
05 荷尔蒙和母性行为
非人类动物研究提供了对母性行为的激素调节的深刻理解。母亲行为的体液基础最早的证据之一可以追溯到1972年。Terkel和rosenblattt将怀孕的动物血液输入非母性处女雌性,导致后者迅速诱导母性行为。此外,接受雌二醇、黄体酮和催乳素激素治疗的卵巢切除的雌性处女将其表现为母性的潜伏期从典型的6-7天减少到35-40小时。此外,较新的研究使用条件转基因。研究方法发现,雌激素和催乳素促进母性行为的作用可能是通过位于内侧视前区(MPOA)的特定受体介导的,MPOA是母性脑回路的中心区域。除了这些激素,其他几项研究表明,催产素在刺激母性行为方面还起着额外的作用。具体地说,催产素和雌二醇的组合可以刺激去卵巢的雌性大鼠的母性行为,而单独使用催产素则需要更长的时间来诱导母性反应。最后,皮质酮管理调节了肾上腺切除的母性行为的强度。这些发现表明围产期类固醇(雌二醇、孕酮和皮质酮)和肽激素(催产素和催乳素)共同促进和调节产妇行为。在人类中,将激素和母性行为联系起来的证据很少,而且是基于相关数据的。此外,文献主要集中在一种激素:催产素。与在其他哺乳动物中观察到的情况类似,在怀孕和产后期间测量的外周催产素水平与母性行为有关。其中包括母婴同步的增加。敏感的母性、积极的沟通和深情的接触。然而,应该指出的是,来自下丘脑的催产素可能对母性行为产生更大的影响。
除了催产素,还有一些较少被探索的激素与人类母性关怀的表达有关。例如,在妊娠早期和晚期,雌二醇和黄体酮的激素变化与母亲更高的敏感性、亲昵接触、缺乏侵入性以及产后对新生儿更积极的依恋感有关。在产后早期,研究还发现,较高的血浆皮质醇水平与母亲被新生儿气味所吸引的感觉有关。在产后早期,当皮质醇恢复到孕前水平时,母亲较低的皮质醇似乎与母亲在与婴儿玩耍时较高的敏感性呈正相关。最后,在哺乳期,喂养婴儿后的高催乳素水平与母亲在与婴儿互动时表现出更高的敏感性呈正相关。
MRI研究显示怀孕前后灰质的结构变化。左侧表示怀孕期间观察到的灰质体积减少。右侧为产后观察到的灰质体积总体增加。下图:时间线显示妊娠期间理想的基础激素水平。出生和产后时期。插图说明了催乳素和催产素在母乳喂养期间观察到对母乳喂养反应的波动,每个峰值对应于一次母乳喂养。这些理想化的轨迹是根据在怀孕或产后多个时间点测量激素的研究汇编而成。
06 母体回路的激素控制
尽管有上述证据,但怀孕激素促进人类母性行为的大脑机制仍然未知。幸运的是,产妇行为是一个多因素结构,并不完全依赖于激素刺激。母性行为的神经生物学基础在小鼠模型中得到了广泛的研究,从而提供了一个参考框架。接下来,我们将提供啮齿动物母性大脑文献的概述,作为推断激素如何激活特定大脑网络以引发人类母性行为的路线图。
6.1 啮齿类动物母系回路的激活
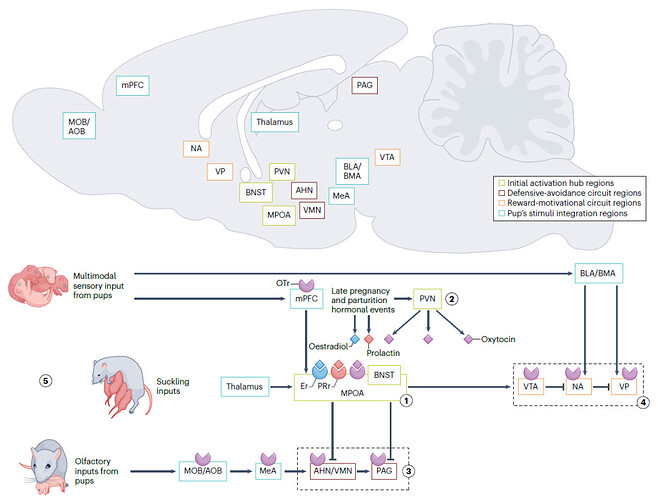
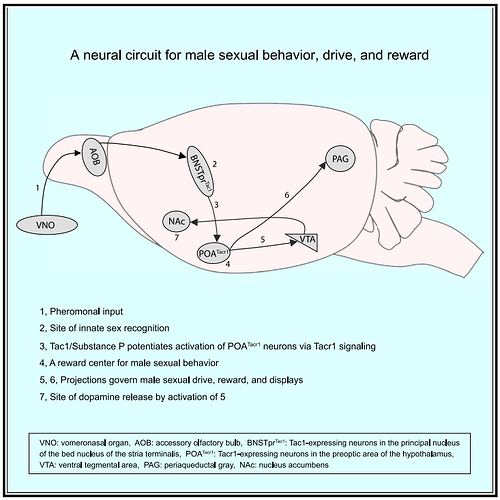
在大鼠中,围产期激素靶向激素敏感的神经区域来启动母性行为(图3)。在分娩前孕酮水平下降后,雌二醇和催乳素与下丘脑吻侧MPOA中的受体结合。该地区被认为是产妇行为开始的最初中心。在不同的MPOA神经元群体中,小鼠的光遗传学研究强调了表达MPOA丙氨酸的神经元在控制亲代行为中的作用。
在与特定的MPOA受体结合后,雌二醇和催乳素激活细胞质激酶级联反应和基因组信号通路,从而产生功能活跃和对幼崽有反应的MPOA神经元。细胞质和基因组机制导致两种类型的大脑可塑性:分子和结构。分子可塑性包括增加神经递质、神经调节剂和受体水平,以调节神经电活动。结构可塑性影响神经元形态,包括体细胞大小、“树突”长度、分支和“脊柱”密度的变化。与此同时,来自下丘脑室旁核的催产素到达母体回路的多个区域,包括MPOA、mPFC、BNST、腹侧被盖区、伏隔核、腹侧白球、嗅球和杏仁核”。在这些大脑区域,催产素通过激励和指导大坝的行为。在神经层面上,这涉及到防御-回避神经回路的抑制和奖励-动机神经回路的刺激。MPOA投射抑制防御-回避回路,该回路涉及从嗅球到内侧杏仁核的投射,然后通过下丘脑的前核和腹内侧核到导水管周围灰质。随着防御回避回路的抑制,MPOA的激素激活通过刺激从腹侧被盖区向伏隔核释放多巴胺来调动奖励动机回路。多巴胺对伏隔核壳DI受体的作用增加了腹侧腭对来自基底外侧和基底内侧杏仁核的小波刺激的反应性。从腹侧苍白球到其他基底神经节和运动区域的投射是引发产妇接近行为的关键。
一旦母性回路被妊娠晚期和分娩激素激活,母性行为已经建立,母性行为就会通过幼崽的感觉相关输入来维持和适应。嗅觉、触觉、哺乳和视觉刺激首先由初级感觉皮层处理。然后,这些信息被整合到丘脑和联合皮层,如mPFC,并被整合到母体回路的关键节点,如MPOA和杏仁核(基底外侧核、基底内侧核和内侧核)。这个过程反馈到回路中,以维持和调整母性行为,以适应产后幼犬的需要。除了母脑回路的关键区域外,海马体和mPFC等其他区域也会影响母脑的行为,分别调节与空间学习和记忆有关的方面,并帮助组织和认知灵活性来照顾母脑。
上图:鼠脑矢状切面,显示构成母性回路的主要区域。作为电路初始枢纽的区域用绿色表示。奖励动机和防御回避子回路的区域分别用橙色和栗色表示。接收幼崽感官输入的区域用蓝色表示。下图:啮齿类动物母性回路的示意图,包括上图的大脑区域,以及孕晚期和分娩激素的受体和激活受体:雌二醇(蓝色)、催乳素(红色)和催产素(紫色)。值得注意的是,除了MPOA外,雌激素-催乳素受体也在其他脑区表达。
6.2 人类母体回路的激活
人类的母体电路不仅共享啮齿动物网络的核心区域,而且还包括后来进化的人类特有的成分。功能性磁共振研究表明,人类母性行为是由一个高度保守的哺乳动物皮层下网络控制的,该网络通过多个投射与后期进化的皮层网络相连,该网络涉及高阶社会情感功能。与啮齿类动物相似,人类母亲的皮层下区域通常被激活,以响应婴儿的信号,包括下丘脑、杏仁核和多巴胺能奖励区,如伏隔核和腹侧被盖区。这种网络可能维持了哺乳动物中高度保守的亲代行为的某些方面,如对婴儿的警惕和奖励。除了皮层下网络,暴露于婴儿相关刺激的人类母亲的皮层区域也会被激活。这些区域通常包括前扣带皮层、脑岛、mpfc和颞顶叶交界处。这些大脑区域与父母的关键认知过程有关,比如同理心。心智化和情绪调节人类大脑中属于母体回路的区域含有丰富的“妊娠激素”受体。死后研究报道了下丘脑中雌激素、催乳素和催产素受体的mRNA表达。除了这些区域,研究人员还报道了杏仁核和前扣带皮层中催产素受体的mRNA表达。这加强了人类使用与啮齿动物相似的激素途径来促进母性行为的可能性。在下一节中,我们将讨论在啮齿动物中发现的激素诱导的神经可塑性过程可能是在人类中观察到的神经解剖学变化的基础。
07 激素与神经可塑性
激素介导的啮齿动物母脑可塑性涉及多个尺度的变化,从分子到细胞和形态的变化。后两者被称为结构可塑性。结构可塑性涉及神经或神经胶质形态的改变以及神经元和神经胶质脑细胞数量的更大规模变化。包括神经发生减少和小胶质细胞的增殖,以及髓磷脂生成和修复的增加。在这里,我们关注的是影响脑细胞形态和数量的大脑结构可塑性变化,因为这种形式的可塑性比分子水平的变化更有可能影响神经解剖学。我们主要讨论来自大鼠的研究结果,因为它们是研究得最好的啮齿动物,以了解母体大脑的结构可塑性。
7.1 激素介导的神经可塑性
7.1.1 神经发生
大鼠围生期伴有海马齿状回和侧脑室室下区神经发生的变化。关于心室下区,小鼠研究的有力证据表明,怀孕期间催乳素的激增促进了该区域的神经发生。这些神经元随后迁移到嗅球,可能有助于识别熟悉的气味并促进母性行为。海马神经发生对母性行为的影响还没有得到很好的理解。然而,在本节中,我们将重点放在海马体上,因为它是目前唯一被证实在人类中有神经发生的大脑区域。未来的研究应该检查在人类怀孕期间其他部位发生神经发生的可能性。
研究表明,与未产大鼠相比,在向母性过渡的过程中,包括妊娠中期和晚期早期、中期和产后后和断奶,母鼠的海马细胞增殖减少。从产后中期开始,海马增殖细胞的存活率也降低了。在非生殖条件下,海马神经发生通常由雌二醇刺激而由皮质酮抑制。然而,对怀孕期间神经发生激素相关性的研究发现,神经发生与雌二醇水平之间没有关联。相反,产后海马神经发生的减少与雌二醇水平的下降以及与哺乳期相关的皮质酮水平的持续下降有关。因此,围产期类固醇激素波动可能抑制雌性大鼠妊娠中期至产后后期海马神经发生。
7.1.2 神经元形态
妊娠期和产后大鼠母脑回路,包括皮质下(MPOA和下丘脑视上核、海马和伏隔核)和皮质区(mPFC和扣带皮层),在体细胞大小、树突长度、分支数和树突棘数等方面发生了神经元形态学变化。
与未生育大鼠相比,妊娠后期妊娠大鼠海马CA1神经元的树突棘密度增加,海马CA3神经元的树突复杂性降低(交叉点减少)。怀孕大鼠mpo动脉瘤内的体大小、树突长度和树突分支也增加,在产后早期恢复到基础状态。在产后早期到中期,雌性大鼠海马、伏隔核、mPFC和扣带皮层的树突棘密度增加。在产后早期和中期,MPOA、伏隔核和mPFC的树突长度和树突化也增加,尾状核和下丘脑视上核的树突长度和树突化减少。mPFC脊柱密度在产后后期和断奶前后保持增加,但此后下降。在海马中,脊柱密度在产后后期和断奶后似乎没有改变,尽管其他研究报道在断奶前后和之后海马脊柱密度增加。断奶时,mPFC的树突长度和分支正常化,而海马的树突长度和分支减少妊娠晚期类固醇激素似乎在这些形态学变化中起着重要作用。孕酮和雌二醇模拟妊娠的管理不仅促进了母性行为,而且还产生了与产后观察到的大坝相似的神经元形态变化:海马和树突棘密度增加长度、分支和躯体大小在MPOA中扩展。断奶后,雌二醇和皮质酮与海马树突分支均无相关性。重要的是,在整个怀孕过程中,雌二醇和黄体酮促进MPOA周围神经网的逐渐形成。这些细胞外蛋白包围着神经元,在神经可塑性阶段稳定神经连接。因此,妊娠类固醇激素可能激活雌性啮齿动物妊娠后期母体脑回路中的树突生长并巩固神经回路。
08 激素介导的神经胶质可塑性
母亲大脑的可塑性并不局限于神经元。包括小胶质细胞、少突胶质细胞和星形胶质细胞在内的上皮细胞的修饰也有文献记载。我们提供的主要机制的概述,其中胶质细胞已被发现产生结构脑变化的雌性大鼠在围产期。这些机制包括小胶质细胞增殖减少,髓鞘形成和星形胶质细胞重塑增加。
8.1 小胶质细胞的变化
转变为母亲似乎改变了大脑固有的免疫细胞,小胶质细胞。小胶质细胞作为巨噬细胞清除微生物、细胞碎片和dea神经元,是大脑细胞因子分泌的主要来源,因此促进了神经炎症过程。此外,小胶质细胞通过动态调节突触可塑性在塑造神经网络中也很重要[0-94]。与未孕大鼠相比,妊娠后期(妊娠第20天)和产后早期(产后第1、8天)小胶质细胞密度较低,断奶后则相反。这些小胶质细胞的减少特别影响母体回路,包括海马体、伏隔核、杏仁核和mPFC。
到目前为止,尚无直接证据表明妊娠激素与小胶质细胞减少有关。然而,小胶质细胞具有妊娠相关激素的受体,其水平在妊娠后期的不同阶段达到峰值,如糖皮质激素、雌激素、黄体酮和催产素。这些激素已被发现可减轻小胶质细胞诱导的神经炎症,并促进小胶质细胞增殖以保护神经元免受延长的神经炎症。因此,这些激素可能是怀孕期间和产后观察到的小胶质细胞数量下调的基础。值得注意的是,小胶质细胞数量的减少是由于小胶质细胞增殖的减少,并且是特异性的,这些小胶质细胞通常会调查环境中的碎屑或病原体。这表明围生期神经免疫监测可能减弱。事实上,对免疫挑战的神经免疫反应在母体大脑中被抑制,特别是在围产期。这些发现表明,至少在啮齿类动物中,怀孕相关激素可能有助于怀孕期间的小胶质细胞适应。
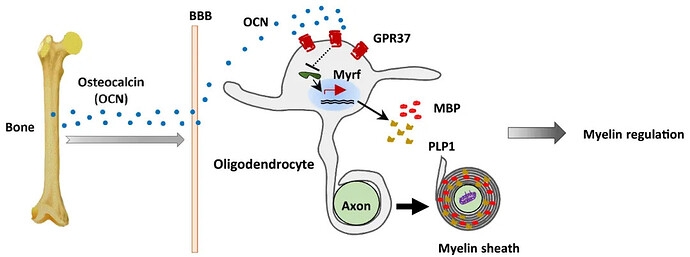
8.2 髓鞘形成
大鼠研究报告了与妊娠相关的oli goddercytes的变化,这是一种负责神经元轴突髓鞘形成的脑细胞。具体来说,少突胶质细胞祖细胞在妊娠期、哺乳期加速其增殖和成熟少突胶质细胞的数量。结果,有髓鞘轴突的数量增加,表明在啮齿动物的母体大脑中有髓鞘形成的能力增强。妊娠也能促进大鼠脑白质损伤后的髓鞘再生或髓鞘修复。这些与妊娠相关的促髓鞘形成过程,至少部分是由于孕酮诱导的gaba能张力增强。催乳素激素也被证明可以促进小鼠怀孕期间少突胶质细胞的产生,导致啮齿类动物母体大脑髓鞘形成增加,但尚未在大鼠模型中进行研究。因此,妊娠激素可以增加雌性啮齿动物的髓鞘形成能力。
8.3 星形改造
最后,大鼠向母性的转变还需要星形胶质细胞的形态学改变,星形胶质细胞是调节突触功能的胶质细胞。这些变化发生在大脑的一些区域,比如扣带皮层和下丘脑区域。在大鼠中,从妊娠晚期到哺乳期,扣带皮层和MPOA显示出星形细胞形态标志物的增加,如胶质活化碱性成纤维细胞生长因子(bFGF)和星形细胞细胞骨架胶质纤维酸性蛋白。研究表明,类固醇激素和母体经验相互作用可诱导星形胶质细胞。
Ence在未交配大鼠的扣带皮层中产生了类似的星形细胞变化。扣带皮层的可塑性。具体来说,孕酮和雌二醇的方案模拟怀孕和3小时的产妇经验星形细胞形态的改变也发生在另一个下丘脑核:视上核。在基础条件下,下丘脑视上核表达催产素的神经元高度堆积,但仍被星形细胞过程分开。
大鼠在分娩前后,下丘脑视上核表达催产素的细胞中的星形细胞覆盖明显减少,导致细胞体与树突直接接触。这种星形细胞收缩被认为在此期间上调催产素分泌。因此,大鼠研究表明,妊娠激素通过星形细胞可塑性调节母体回路关键节点的突触传递。
总体而言,啮齿动物研究提供证据表明,怀孕相关的激素波动减缓神经发生,激活树突生长,改变大脑免疫功能,促进髓鞘形成,并通过影响神经元和胶质细胞的可塑性过程调节突触传递。这些过程在怀孕后期尤为突出,有助于在产后重塑母亲的大脑。
09 MRI观察神经可塑性
前面的章节已经回顾了分析大脑可塑性的细胞和形态标记的离体组织学研究。然而,使用MRI的体内神经解剖学测量也可以在宏观水平上阐明神经可塑性过程。不幸的是,核磁共振研究很少证实与妊娠激素有关。在怀孕的大鼠中,MRI只应用了基于扩散的MRI,它通过测量组织内水的扩散特性来捕捉大脑的微观结构排列。特别是,一项纵向研究发现,怀孕后期的大鼠的灰质和白质扩散增加,这表明在怀孕期间,脑组织微观结构对水分子的扩散运动变得更容易渗透。此外,在小鼠中,12只小鼠的纵向MRI研究显示,在产后期间,母亲的多个大脑区域(包括MPOA、BNST、室旁下丘脑核、尾核、壳核、杏仁核、岛和海马)的灰质瞬间增加。其中一些灰质的增加开始于妊娠后期,包括MPOA、BNST和脑岛,这与在人类中观察到的总体下降趋势形成了对比。这种不一致可能是由于所研究的特定大脑区域(皮层下与皮层)的差异以及成像获取参数和处理管道的差异。此外,人类神经成像研究主要包括全脑分析,这可能掩盖特定区域的趋势。最后,在将啮齿动物的研究结果应用于人类时,围产期激素环境的细微差异以及母亲需求的差异也应被考虑在内。到目前为止,还需要进一步的研究来确定啮齿动物怀孕引起的灰质变化是否与人类观察到的相似。在人类中,在过渡到母亲的过程中,灰质体积的动态轨迹伴随着母亲在分娩前后经历的激素变化(图2)。灰质体积的减少被认为发生在怀孕期间催乳素和类固醇激素(黄体酮、雌二醇和皮质醇)正在稳步增加。相比之下,产后灰质体积的增加与类固醇激素的急剧下降以及与哺乳和母婴接触有关的催产素和催乳素脉冲一致。这个时间线支持了激素可能直接或间接与人类大脑结构变化有关的假设。尽管我们有证据表明怀孕激素会到达大脑,但它们如何影响与怀孕相关的神经可塑性和母亲的行为尚不清楚。在下一节中,我们将讨论这种关系如何基于前几节所回顾的证据,并提出未来研究的方向。具体地说,我们讨论了妊娠相关激素可能协调促进人类母性行为的神经可塑性变化的潜在途径。
10 未来的发展方向
在前面的章节中,我们概述了与内分泌系统如何刺激神经可塑性以启动和维持母性行为相关的人类和啮齿动物研究。我们关注激素作为母体神经可塑性的主要激发子,并采用多尺度视角描述从分子过程到整个脑组织的神经可塑性。在最后一节中,我们将讨论哪些神经可塑性过程可能导致MRI检测到的人类神经解剖学变化,以及它们与妊娠激素和母亲行为的关系。我们还概述了目前人类研究的局限性,并提出了未来在母体大脑领域的研究问题。
10.1 支撑细胞机制
考虑到标准的MRI分辨率,在人类中观察到的大规模灰质体积变化不太可能仅仅是由形态学和分子水平上的神经可塑性产生的。相反,影响脑细胞增殖的较大变化可能是导致体积变化的主要因素。因为在人类母亲中检测到的神经解剖学变化是动态的(即,怀孕期间灰质减少,产后灰质增加),再生缓慢的脑细胞,如神经元,不太可能支持这些变化。此外,人类成人的神经发生只在海马体中被观察到,一个更可能的候选者是小胶质细胞,它在整个大脑中表现出更高的再生率。
尽管已经发现在大鼠母体关键脑回路中发生的小胶质细胞变化遵循与人类观察到的灰质变化相似的动态轨迹,但未来的研究应该解决小胶质细胞在人类妊娠相关神经解剖学变化中的作用。值得注意的是,肌醇水平的改变。然而,这些代谢生命变化的确切方向和时间模式需要根据相互矛盾的结果进一步研究。例如,Hoekzema等人报告了从孕前到产后早期肌醇水平的增加,而Nelander等人表明妊娠后期肌醇水平下降。更高的MRI数据采样率将有助于更准确地描绘灰质轨迹,并确定特定的转折点。此外,未来的研究应应用优化的MRI标记物来靶向小胶质细胞的活动或增殖,以帮助确认小胶质细胞对妊娠期间灰质变化的贡献。此外,由于小胶质细胞是一种免疫能力细胞。
研究神经胶质标志物以及免疫活动的外周和中枢标志物,监测具有非典型免疫环境的妊娠,如多发性硬化症和通过捐赠卵子怀孕,将是一件有趣的事情。如果这些标志物的动态变化与孕期和产后灰质变化的演变有关,我们可能有间接证据表明免疫对这些变化有贡献。
除了小胶质细胞的变化外,髓鞘形成也被认为通过将组织界面的体素错误地分类为白质而诱导灰质的明显减少。然而,在人类中,少数几项关于怀孕引起的白质变化的研究并没有发现明显的影响。此外,尽管横断面研究表明孕妇和非孕妇的脑灌注没有差异,但需要进行纵向研究,以排除伴随妊娠的明显血管适应在MRI变化中的潜在贡献。
10.2 荷尔蒙系统的作用
怀孕期间的荷尔蒙波动超过了女性生命中任何其他时期的水平,预计在诱导妊娠相关的神经可塑性方面起着主要作用。然而,在人类中,很少有研究将神经解剖学的变化与这一生命阶段的荷尔蒙气候相协调。最近,Hoekzema等人研究了雌二醇、雌三醇、黄体酮和皮质醇与初为人母的大脑结构重组的关系。在这项研究中,只发现妊娠后期雌二醇水平与整个妊娠期间观察到的灰质体积减少呈正相关,这表明这种类固醇激素有助于人类大脑结构重组。然而,尚不清楚其他未经测试的激素或特定的激素比例是否也可能导致观察到的母体大脑结构变化。
鉴于激素的相互作用性质,神经解剖学的改变很可能不依赖于独立的激素效应,而是依赖于多种类固醇激素和肽激素之间复杂的相互作用。怀孕期间和产后期间的激素环境比少数活性激素的存在要复杂得多。如前所述,在怀孕期间和产后早期,这种环境是动态的(图2)。此外,胎盘独特的激素和酶组成导致母体循环中存在的活性成分发生实质性改变。这些改变包括激素水平的变化,不同激素和代谢物之间的平衡,甚至是怀孕时产生的激素相关代谢物,如雌三醇和人类胎盘乳原。例如,虽然还没有与母体大脑的神经可塑性联系起来,但雌三醇和人类胎盘的乳酸水平在怀孕期间会大幅增加,并且可以通过与雌二醇和催乳素相同的受体起作用。因此,在怀孕期间观察到的人类大脑的变化可能是由激素和代谢物的动态鸡尾酒引起的。
为了更好地理解这种复杂的环境是如何导致观察到的大脑变化的,未来的研究应该在母性转变的不同时间点评估更多的激素和代谢物以及MRI数据。此外,由于测量大脑内激素变化的侵入性,人类研究依赖于外周激素水平来解释激素波动与观察到的大脑变化之间的潜在联系。因此,未来的研究应更好地阐明外周和中枢激素变化的关系人类和非人类物种,尤其是关键怀孕神经肽,如催产素和催乳素。
10.3 与母性行为有关
大脑结构的改变——可能是由细胞水平的神经可塑性过程支持的——可能只间接影响母性行为。相反,影响神经元活动和形态的神经可塑性变化可能与母性行为有更直接的关系。在啮齿类动物的研究中,伴随母性护理出现的分子和形态神经可塑性事件与调节控制母性护理的神经回路的连通性和兴奋性有关。反过来,细胞可塑性可能通过确保分子和形态变化的最佳发生而与母性行为间接相关,从而确保母性回路的正确功能。事实上,在妊娠后期和产后早期,小胶质细胞的耗竭模拟了小胶质细胞张力的降低,从而促进了处女雌性动物的母性行为。小胶质细胞的减少究竟是如何塑造母体神经回路的尚不清楚。一种可行的方法是创造一个较少炎症和更容易兴奋的环境,有利于大脑的重塑。
在人类中,与怀孕相关的神经解剖学变化与母亲行为的不同方面(例如,母亲对婴儿的依恋质量)之间的联系很少,有时无法复制。未来的研究应该评估不同大脑指标(包括功能、解剖、扩散或光谱数据)的变化如何相互作用,以促进人类的母性行为。这些研究将阐明大脑结构改变如何转化为功能调整,并促进母性行为。这些调查应该积极促进正在进行的母性重塑,将其描绘为大脑不断适应的阶段,从而消除母亲大脑功能失调或bl2不足的过时观念。
对于推断母亲行为的指标,我们认为具有更高生态效度的指标可以使该研究领域受益。在人类中,研究分析了与向母亲过渡相关的神经解剖学变化,通过问卷间接推断了母性行为。虽然这些可以帮助我们理解母亲对母性的主观体验,但它们也受到“社会可取性偏见”的影响,这可能会扭曲他们的解释。未来的研究应该包括在更自然的环境中测量母亲的行为,使用诸如静止面孔范式、陌生情境或自由玩耍等范式。这将使我们能够更好地推断亲子关系的质量,并将大脑的变化与母性行为的不同组成部分联系起来。
10.4 外在因素的贡献
人类母性行为可能取决于内在的妊娠因素和外在的产后因素的结合。外在因素不仅包括与婴儿的持续互动,这可能导致经验诱导的神经可塑性,还包括母乳喂养的类型、睡眠、压力、水合作用、体重和营养。外在因素可能通过产妇护理回路中的亚细胞神经可塑性过程而不是通过神经解剖学改变来塑造产妇行为。由于人类的亲代养育高度依赖于社会文化因素,因此研究控制性别和潜在的性别角色对儿童养育的作用对于理清妊娠和儿童养育因素的贡献是重要的。加入包括同性伴侣或养父母在内的非妊娠父母组将捕捉到产后外在因素的影响,同时也排除了性别和性别的潜在影响。
11 结论
总之,我们目前依靠的一些证据激素在激活和调节神经可塑性过程在怀孕和产后期间的作用。然而,需要更多的研究来阐明在人类向母性过渡过程中涉及的神经可塑性过程的类型以及它们如何影响母性行为。目前的前沿是细胞和亚细胞的神经可塑性如何影响神经元和神经胶质细胞塑造人类的母性行为。未来的研究应该解决这些问题,以阐明激素和环境因素如何触发支持人类适应性母性行为的神经调节。